题目内容
13.有一种银锌电池,其电极分别为Ag2O和ZnO,电解质溶液为KOH,电极反应式分别为:Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-,根据上述电极反应式,下列说法正确的是( )
| A. | Zn是正极,Ag2O是负极 | |
| B. | 使用过程中,电子由Ag2O极经外路流向Zn极 | |
| C. | 使用过程中,电极负极区溶液的pH减小 | |
| D. | Zn电极发生氧化反应,Ag2O电极发生还原反应 |
分析 A.电池反应中Zn元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,所以Zn是负极、Ag2O是正极;
B.该原电池中,Zn是负极、Ag2O是正极,电子从负极沿导线流向正极;
C.根据元素化合价变化知,Zn失电子而作负极,负极上OH-参加反应导致其浓度减小;
D.失电子的物质发生氧化反应、得电子的物质发生还原反应.
解答 解:A.电池反应中Zn元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,所以Zn是负极、Ag2O是正极,故A错误;
B.该原电池中,Zn是负极、Ag2O是正极,电子从负极Zn沿导线流向正极Ag2O,故B错误;
C.根据元素化合价变化知,Zn失电子而作负极,负极上OH-参加反应导致其浓度减小,溶液的碱性降低,pH减小,故C正确;
D.Zn失电子发生氧化反应、Ag2O得电子发生还原反应,故D错误;
故选C.
点评 本题考查化学电源新型电池,侧重考查分析判断能力,明确元素化合价变化与电极关系是解本题关键,知道各个电极上反应类型、电子及电流流向,题目难度不大.

练习册系列答案
相关题目
1.在1L密闭容器内,一定条件下发生A+3B?2C反应,在10s内,反应物A的浓度由2mol降到1.2mol,则C的反应速率为( )
| A. | 1.6 mol/(L•s) | B. | 0.08 mol/(L•s) | C. | 0.16 mol/(L•s) | D. | 0.8 mol/(L•s) |
8.下表是元素周期表的一部分,回答下列问题:
(1)写出②⑧⑩三种元素分别为N;Si;S.
(2)写出①、③两种元素形成的化合物有两种,化学式:CO,CO2.
(3)写出①元素最高价氧化物的电子式和结构式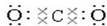 ,O=C=O.
,O=C=O.
(4)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;NaOH碱性最强;能形成两性氢氧化物的元素是Al.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | O |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)写出①、③两种元素形成的化合物有两种,化学式:CO,CO2.
(3)写出①元素最高价氧化物的电子式和结构式
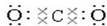 ,O=C=O.
,O=C=O.(4)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;NaOH碱性最强;能形成两性氢氧化物的元素是Al.
18.把0.02mol/L CH3COOH溶液和0.01mol/LNaOH溶液等体积混合,溶液呈酸性,则混合溶液中微粒浓度关系不正确的是( )
| A. | c(CH3COO-)>c (Na+) | B. | c(CH3COOH)+c(CH3COO-)=0.02mol/L | ||
| C. | c(CH3COOH)<c(CH3COO-) | D. | c(CH3COO-)+c(H+)=c (Na+)+c(OH-) |
2.向1L 0.1mol/L的Na2SO3溶液中滴加盐酸(假设反应前后溶液体积不变),溶液中水电离出的OH-离子浓度随盐酸的用量关系如图所示.图中各点溶液pH随n(SO32-):n(HSO32-)变化关系如下表,下列叙述不正确的是( )


| 坐标对应点 | a | b | c | d |
| n(SO32-):n(HSO32-) | / | 91:9 | 1:1 | 9:91 |
| pH | >8.2 | 8.2 | 7.2 | 6.2 |
| A. | b点溶液中:水电离出的c(OH-)=1×10-5.8mol/L | |
| B. | c点溶液中:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+) | |
| C. | d点溶液中HSO3-的电离大于水解 | |
| D. | d点溶液中:c(Na+)<c(SO32-)+c(HSO3-)+c(Cl-) |
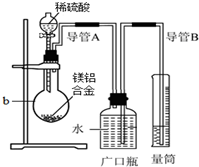 化学学习小组对某镁铝合金进行了如下实验研究,请你参与并完成对有关问题的解答.
化学学习小组对某镁铝合金进行了如下实验研究,请你参与并完成对有关问题的解答.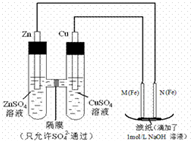 某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.
某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.