题目内容
20.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将少量Fe(NO3)2加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成血红色 | Fe(NO3)2已变质 |
| B | 在KI溶液中滴加少量氯水,再加入CCl4,充分震荡. | 液体分层,下层溶液呈紫红色. | 氯的非金属性比碘强 |
| C | 炭粉中加入浓硫酸并加热,导出的气体通入BaCl2溶液中 | 有白色沉淀产生 | 有SO2和CO2产生 |
| D | 向AgNO3溶液中滴加少量NaCl溶液,然后再向其中滴加KI溶液 | 先生成白色沉淀,后生成黄色沉淀 | 溶解度:AgCl>AgI |
| A. | A | B. | B | C. | C | D. | D |
分析 A.水溶液后加稀硫酸酸化,酸性条件下亚铁离子、硝酸根离子可发生氧化还原反应;
B.下层溶液呈紫红色,说明有碘单质生成,从而可证明氯气的氧化性大于碘单质;
C.二氧化碳、二氧化硫都不与氯化钡溶液反应;
D.实现了沉淀的转化,溶度积越小溶解度越小,越容易生成沉淀.
解答 解:A.加水溶液后加稀硫酸酸化,酸性条件下亚铁离子、硝酸根离子可发生氧化还原反应,应溶于水滴加KSCN溶液,溶液变为红色检验是否变质,故A错误;
B.在KI溶液中滴加少量氯水,再加入CCl4,充分震荡后液体分层,下层溶液呈紫红色,碘化钾为氧化成碘单质,说明氯气的氧化性大于碘单质,从而可证明氯的非金属性比碘强,故B正确;
C.炭粉中加入浓硫酸并加热,由于SO2和CO2不与氯化钡溶液反应,将导出的气体入BaCl2溶液中不会生成白色沉淀,故C错误;
D.向AgNO3溶液中滴加少量NaCl溶液,然后再向其中滴加KI溶液,先生成白色沉淀,后生成黄色沉淀,说明AgI更难溶,溶度积越小其溶解度越小,则溶解度:AgCl>AgI,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、离子检验、沉淀的转化及实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
10.银器久置变黑多是表面生成银锈Ag2S所致.用铝制容器配制含小苏打和食盐的稀溶液,将变黑银器浸入溶液中,并使银器与铝制容器接触,一段时间后,黑锈褪去,而银却极少损失.上述过程中,起还原作用的物质是( )
| A. | Ag2S | B. | NaCl | C. | Al | D. | NaHCO3 |
11.下列与有机化合物相关的说法正确的是( )
| A. | 淀粉、油脂、蛋白质都能水解,但水解产物不同 | |
| B. | 甲烷和Cl2、乙烯和Br2的反应类型相同 | |
| C. | 1mol 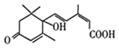 与足量Na反应生成2molH2 与足量Na反应生成2molH2 | |
| D. | 分子式为C4H10O,含有“-CH2OH”的有机物的同分异构体有3种(不考虑立体异构) |
8.漂粉精的有效成分是( )
| A. | Ca(ClO)2 | B. | CaCl2 | C. | CaCO3 | D. | Ca(OH)2 |
12.有机物  常用作合成中间体.下列有关该有机物的叙述中正确的是( )
常用作合成中间体.下列有关该有机物的叙述中正确的是( )
 常用作合成中间体.下列有关该有机物的叙述中正确的是( )
常用作合成中间体.下列有关该有机物的叙述中正确的是( )| A. | 可由丙烯与Cl2发生加成反应制得 | B. | 分子式为 C5H10Cl2 | ||
| C. | 还有3种同分异构体 | D. | 分子中所有碳原子不可能共平面 |
9.下列有关离子大量共存或离子方程式书写正确的是( )
| A. | c(I-)=0.1mol/L 的溶液中:K+、Na+、SO42-、ClO- | |
| B. | 常温下,通入SO2气体的溶液中:Al3+、Ca2+、MnO4-、Cl- | |
| C. | 控制pH为9-10,用NaClO溶液将含NaCN废水中的CN-氧化为两种无污染的气体:2CN-+5ClO-+H2O═N2↑+2CO2↑+5Cl-+2OH- | |
| D. | 向含有Ba2+、Cl-、HCO3-的离子组中加入少量的NaOH溶液:HCO3-+OH-═CO32-+H2O |
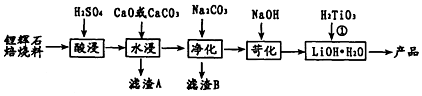
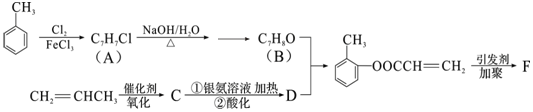
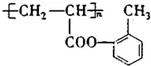
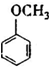 (填结构简式).
(填结构简式).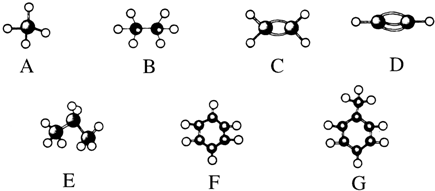
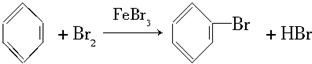 .
.