题目内容
下列电离方程式错误的是( )
| A、H2CO3?2H++CO32- |
| B、NaHSO4(溶液)=Na++H++SO42- |
| C、NaHCO3=Na++HCO3- |
| D、Ba (OH)2=Ba2++2OH- |
考点:电离方程式的书写
专题:
分析:A.多元弱酸分步电离,以第一步为主;
B.硫酸是强电解质,硫酸氢根离子在溶液中能完全电离出氢离子和硫酸根离子;
C.碳酸氢钠为强电解质,在溶液中电离出钠离子和碳酸氢根离子,弱酸酸根碳酸氢根离子不能拆写;
D.氢氧化钡为强电解质,完全电离,用等号连接;
B.硫酸是强电解质,硫酸氢根离子在溶液中能完全电离出氢离子和硫酸根离子;
C.碳酸氢钠为强电解质,在溶液中电离出钠离子和碳酸氢根离子,弱酸酸根碳酸氢根离子不能拆写;
D.氢氧化钡为强电解质,完全电离,用等号连接;
解答:
解:A.碳酸为多元弱酸,分步电离,电离方程式为H2CO3?H++HCO3-、HCO3-?H++CO32-,故A错误;
B.NaHSO4为强电解质,在水中完全电离,电离方程式为:NaHSO4=Na++H++SO42-,故B正确;
C.NaHCO3是强电解质,能完全电离,电离方程式为NaHCO3═Na++HCO3-,故C正确;
D.氢氧化钡是强碱,为强电解质,完全电离,电离方程式为:Ba(OH)2 =Ba2++2OH-,故D正确;
故选A.
B.NaHSO4为强电解质,在水中完全电离,电离方程式为:NaHSO4=Na++H++SO42-,故B正确;
C.NaHCO3是强电解质,能完全电离,电离方程式为NaHCO3═Na++HCO3-,故C正确;
D.氢氧化钡是强碱,为强电解质,完全电离,电离方程式为:Ba(OH)2 =Ba2++2OH-,故D正确;
故选A.
点评:本题考查了电离方程式的书写,侧重基础知识的考查,题目难度不大,注意掌握强弱电解质的概念,明确电离方程式的书写方法,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
合金是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质.分析下表中的数据,不能形成合金的是( )
| Na | Cu | Al | Fe | |
| 熔点/℃ | 97.8 | 1083 | 660 | 1535 |
| 沸点/℃ | 883 | 2567 | 2467 | 2750 |
| A、Cu和Al |
| B、Fe和Cu |
| C、Cu和Na |
| D、Al和Na |
做罐头的马口铁是在铁的表面上镀上一层既耐腐蚀有无毒的锡,但食用时开启后的罐头易生锈,其所发生的反应正确的是( )
| A、负极Sn-2e→Sn2+ |
| B、正极Fe-2e→Fe2+ |
| C、正极2H2O+O2-2e→4OH- |
| D、负极Fe-2e→Fe2+ |
下列化学方程式或离子方程式正确的是( )
| A、用醋酸去除水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | ||
B、甲醛与足量新制Cu(OH)2浊液反应:HCHO+2Cu(OH)2
| ||
C、实验室用液溴和苯在催化剂作用下制溴苯: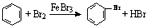 | ||
D、将CO2通入苯酚钠溶液: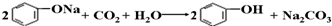 |
下列化学式只能表示一种纯净物的是( )
| A、CF2Cl2 |
| B、C3H6 |
| C、C6H12O6 |
| D、C2H4O2 |
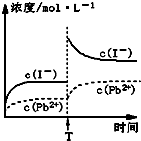 取一定量的PbI2固体用蒸馏水配成饱和溶液,量取25.00mLPbI2饱和溶液,分次慢慢与R-H(s)进行如下反应:Pb2+(aq)+2R-H(s)=R2Pb(s)+2H+(aq),充分反应后,过滤(用锥形瓶盛装滤液),再用蒸馏水洗涤沉淀,将洗涤液一并放在锥形瓶中,加入指示剂,用0.0025mol/LNaOH溶液滴定,当达到滴定终点时,用去氢氧化钠溶液20.00mL.结合上述实验数据,下列有关说法正确的是( )
取一定量的PbI2固体用蒸馏水配成饱和溶液,量取25.00mLPbI2饱和溶液,分次慢慢与R-H(s)进行如下反应:Pb2+(aq)+2R-H(s)=R2Pb(s)+2H+(aq),充分反应后,过滤(用锥形瓶盛装滤液),再用蒸馏水洗涤沉淀,将洗涤液一并放在锥形瓶中,加入指示剂,用0.0025mol/LNaOH溶液滴定,当达到滴定终点时,用去氢氧化钠溶液20.00mL.结合上述实验数据,下列有关说法正确的是( )| A、以酚酞为指示剂时,滴定至终点时溶液由红色变为无色 |
| B、在温度不变时,向PbI2饱和溶液中加入少量硝酸铅浓溶液,PbI2的Ksp减小 |
| C、温度不变,T时刻,向PbI2饱和溶液中加入少量KI浓溶液,离子浓度变化如右图所示 |
| D、本次实验测得的t℃PbI2的Ksp=4×10-9 |
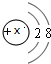 ,则该元素氧化物的化学式为
,则该元素氧化物的化学式为