题目内容
把0.05molNaOH晶体分别加入到下列100mL液体中,溶液导电性变化最大的是( )
| A、0.5mol?L-1NH4Cl |
| B、0.5mol?L-1醋酸 |
| C、0.5mol?L-1H2SO4 |
| D、0.5mol?L-1Cu(NO3)2 |
考点:电解质在水溶液中的电离
专题:
分析:电解质溶液导电性与离子浓度成正比,与离子所带电荷成正比,溶液导电性变化较大,说明溶液中离子浓度变化较大,据此分析解答.
解答:
解:A.氯化铵为强电解质,加入NaOH后生成物仍是强电解质,离子的浓度变化不大,故导电性变化不大,故A错误;
B.醋酸是弱电解质,溶液中氢离子浓度小于0.5mol/L,和NaOH恰好完全反应生成强电解质醋酸钠,溶液中钠离子浓度为0.5mol/L,离子浓度变化较大,溶液导电性变化较大,故B正确;
C.硫酸是强电解质,硫酸中氢离子浓度为0.1mol/L,一半硫酸和NaOH完全反应生成强电解质硫酸钠,溶液中钠离子浓度、氢离子浓度之和仍然为0.5mol/L,离子浓度不变,溶液导电性不变,故C错误;
D.Cu(NO3)2是强电解质,和NaOH恰好完全反应生成强电解质硝酸钠和氢氧化铜沉淀,溶液中钠离子浓度为0.5mol/L,离子浓度不变,溶液导电性不变,故D错误;
故选B.
B.醋酸是弱电解质,溶液中氢离子浓度小于0.5mol/L,和NaOH恰好完全反应生成强电解质醋酸钠,溶液中钠离子浓度为0.5mol/L,离子浓度变化较大,溶液导电性变化较大,故B正确;
C.硫酸是强电解质,硫酸中氢离子浓度为0.1mol/L,一半硫酸和NaOH完全反应生成强电解质硫酸钠,溶液中钠离子浓度、氢离子浓度之和仍然为0.5mol/L,离子浓度不变,溶液导电性不变,故C错误;
D.Cu(NO3)2是强电解质,和NaOH恰好完全反应生成强电解质硝酸钠和氢氧化铜沉淀,溶液中钠离子浓度为0.5mol/L,离子浓度不变,溶液导电性不变,故D错误;
故选B.
点评:本题考查溶液导电性大小判断,明确离子浓度与溶液导电性关系是解本题关键,知道物质的溶解性、电离程度与导电性的关系,题目难度不大.

练习册系列答案
相关题目
向溴化钠、碘化钾的混合溶液中通入过量氯气充分反应,将溶液蒸干,并灼烧所得物质,最后残留的固体物质是( )
| A、NaCl和KCl |
| B、NaCl和KCl和I2 |
| C、NaCl和KI |
| D、NaBr和KCl |
与100mL,2mol/L的AlCl3溶液中Cl-的物质的量浓度相等的是( )
| A、3 mL 2 mol/L的NaCl溶液 |
| B、50 mL 4 mol/L的FeCl3溶液 |
| C、200 mL 1mol/L的HCl溶液 |
| D、50 mL 3 mol/L的BaCl2溶液 |
下列叙述正确的是( )
| A、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应△H>0 |
| B、强电解溶液的导电能力一定强于弱电解质溶液的导电能力 |
| C、CH3COOH、Cu(OH)2、BaSO4、NH3都是常见的弱电解质 |
| D、常温下就能发生的化学反应一定是放热反应 |
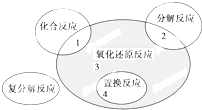
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影3区域的是( )

| A、Cl2+2NaI═2NaCl+I2 | ||||
B、NH4HCO3
| ||||
| C、4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||||
D、Fe2O3+3CO
|
下列物质中含有原子数由多到少排列正确的是( )
①0.1mol H2SO4 ②4.8g氢气 ③5.6L标准状况下NH3 ④4℃时5.4mL H2O.
①0.1mol H2SO4 ②4.8g氢气 ③5.6L标准状况下NH3 ④4℃时5.4mL H2O.
| A、①>②>③>④ |
| B、②>③>④>① |
| C、②>①>③>④ |
| D、③>①>④>② |



 .B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
.B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: