题目内容
用下列各组试剂分离FeCl3和AlCl3两种物质的混合物,其中可以达到目的是
- A.氨水和盐酸
- B.氢氧化钠和二氧化碳
- C.氢氧化钠和盐酸
- D.氨水和二氧化碳
C
分析:A.氨水不能溶解氢氧化铝,无法分离;
B.氢氧化铁、氢氧化铝不能溶解在碳酸中,过滤后不能复原得到FeCl3、AlCl3;
C.加入烧碱会使FeCl3和AlCl3先分别转化为Fe(OH)3和Al(OH)3沉淀,过量加入会使Al(OH)3沉淀转化为可溶的NaAlO2,而Fe(OH)3不会溶解.过滤操作后往Fe(OH)3沉淀加入盐酸会使沉淀溶解再次生成FeCl3;往NaAlO2溶液加入盐酸会先出现Al(OH)3沉淀,盐酸过量沉淀会溶解生成AlCl3,达到分离目的;
D.氨水不能溶解氢氧化铝,无法分离.
解答:A.氨水使两者全部转化为沉淀,氨水属于弱碱,不能使Al(OH)3沉淀转变成偏铝酸盐,无法分离,故A错误;
B.加入烧碱会使FeCl3和AlCl3先分别转化为Fe(OH)3和Al(OH)3沉淀,过量加入会使Al(OH)3沉淀转化为可溶的NaAlO2,而Fe(OH)3不会溶解.过滤操作后,往NaAlO2溶液通入二氧化碳会先出现Al(OH)3沉淀,但碳酸属于弱酸,不能溶解氢氧化铝、氢氧化铁,不能复原得到FeCl3、AlCl3,故B错误;
C.加入烧碱会使FeCl3和AlCl3先分别转化为Fe(OH)3和Al(OH)3沉淀,过量加入会使Al(OH)3沉淀转化为可溶的NaAlO2,而Fe(OH)3不会溶解.过滤操作后往Fe(OH)3沉淀加入盐酸会使沉淀溶解再次生成FeCl3;往NaAlO2溶液加入盐酸会先出现Al(OH)3沉淀,盐酸过量沉淀会溶解生成AlCl3,达到分离目的,故C正确;
D.氨水使两者全部转化为沉淀,氨水属于弱碱,不能使Al(OH)3沉淀转变成偏铝酸盐,无法分离,故D错误;
点评:本题考查物质的分离提纯、铁铝化合物的性质等,难度中等,掌握物质的性质是关键,注意掌握分离提纯原则.
分析:A.氨水不能溶解氢氧化铝,无法分离;
B.氢氧化铁、氢氧化铝不能溶解在碳酸中,过滤后不能复原得到FeCl3、AlCl3;
C.加入烧碱会使FeCl3和AlCl3先分别转化为Fe(OH)3和Al(OH)3沉淀,过量加入会使Al(OH)3沉淀转化为可溶的NaAlO2,而Fe(OH)3不会溶解.过滤操作后往Fe(OH)3沉淀加入盐酸会使沉淀溶解再次生成FeCl3;往NaAlO2溶液加入盐酸会先出现Al(OH)3沉淀,盐酸过量沉淀会溶解生成AlCl3,达到分离目的;
D.氨水不能溶解氢氧化铝,无法分离.
解答:A.氨水使两者全部转化为沉淀,氨水属于弱碱,不能使Al(OH)3沉淀转变成偏铝酸盐,无法分离,故A错误;
B.加入烧碱会使FeCl3和AlCl3先分别转化为Fe(OH)3和Al(OH)3沉淀,过量加入会使Al(OH)3沉淀转化为可溶的NaAlO2,而Fe(OH)3不会溶解.过滤操作后,往NaAlO2溶液通入二氧化碳会先出现Al(OH)3沉淀,但碳酸属于弱酸,不能溶解氢氧化铝、氢氧化铁,不能复原得到FeCl3、AlCl3,故B错误;
C.加入烧碱会使FeCl3和AlCl3先分别转化为Fe(OH)3和Al(OH)3沉淀,过量加入会使Al(OH)3沉淀转化为可溶的NaAlO2,而Fe(OH)3不会溶解.过滤操作后往Fe(OH)3沉淀加入盐酸会使沉淀溶解再次生成FeCl3;往NaAlO2溶液加入盐酸会先出现Al(OH)3沉淀,盐酸过量沉淀会溶解生成AlCl3,达到分离目的,故C正确;
D.氨水使两者全部转化为沉淀,氨水属于弱碱,不能使Al(OH)3沉淀转变成偏铝酸盐,无法分离,故D错误;
点评:本题考查物质的分离提纯、铁铝化合物的性质等,难度中等,掌握物质的性质是关键,注意掌握分离提纯原则.

练习册系列答案
相关题目
在有乙离子存在的情况下,欲用试剂丙来检验溶液中是否含有甲离子,下表所加试剂丙能够对甲离子进行成功检验的是(说明:在实验过程中不允许加热、过滤、萃取等操作)
| 选项 | 试剂丙 | 甲离子 | 乙离子 |
| A | 稀硝酸、BaCl2溶液 | SO42- | SO32- |
| B | AgNO3溶液 | Cl- | I- |
| C | KSCN溶液 | Fe2+ | Fe3+ |
| D | 稀氨水 | Al3+ | Ag+ |
- A.A
- B.B
- C.C
- D.D
已知在常温下,测得浓度均为0.1mol/L的下列六种溶液的pH:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
- A.CO32-+C6H5OH→HCO3-+C6H5O-
- B.CO2+H2O+ClO-→HCO3-+HClO
- C.CO2+H2O+C6H5O-→HCO3-+C6H5OH
- D.CO2+H2O+2C6H5O-→CO32-+2C6H5OH
现有失去标签的6种无色溶液,分别为盐酸、氯化钡、硝酸银、硫酸钠、碳酸钠、硝酸钾溶液.将上述6种溶液两两反应,现象如表所示(↓表示产生沉淀,↑表示产生气体),试推断A、B、C、D、E、F各是上述何溶液(已知Ag2SO4是微溶物,看作沉淀):
| A | B | C | D | E | F | |
| A | ↓ | ↓ | - | ↓ | ↓ | |
| B | ↓ | - | - | ↑ | - | |
| C | ↓ | - | - | - | ↓ | |
| D | - | - | - | - | - | |
| E | ↓ | ↑ | - | - | ↓ | |
| F | ↓ | - | ↓ | - | ↓ |
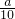 g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol?L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液.
g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol?L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液.