��Ŀ����
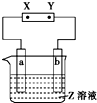
KMnO4�dz��õ�ǿ����������ҵ�������̿���Ҫ�ɷ�MnO2��Ϊԭ�ϣ�ͨ��Һ�෨���������ڼ�������������������MnO2�õ�K2MnO4�������õ�K2MnO4�����ö��Բ���Ϊ�缫���K2MnO4��Һ�õ�KMnO4�����������������£�

��1����Ӧ���з�Ӧ�Ļ�ѧ����ʽΪ�� ��
��2���������������ʹ�ú�MnO280%���ϵĸ�����ΪMnO2������͵�ƶ����Al��Si�������ﺬ���ϸߣ��ᵼ��KOH������ ���ƫ�ߡ���ƫ�͡���������Al���������KOH��Һ��Ӧ�Ļ�ѧ����ʽΪ�� ��
��3�������������ĵ缫��Ӧ����ʽΪ�� ��
��4���ڴ�ͳ�����еõ�K2MnO4��������ͨ��CO2�Ʊ�KMnO4����ѧ��Ӧ����ʽΪ��3K2MnO4+2CO2�T2KMnO4+MnO2+2K2CO3 ����������Ӧ����MnԪ�صĽǶȿ���KMnO4�IJ������Ϊ ����ô�ͳ������ȣ���ⷨ�������� ��
��5���ⶨ���������Ʒ���ȵķ����ǣ�����������Һ�еμ���������Һ������ɫ��������Ӧ�����ӷ���ʽ ��
��6����֪������KSP��Mn��OH��2��=2.0��10-23����ҵ�ϵ���PH������ˮ�е�Mn2+����pH=10ʱ��c��Mn2+��= mol/L��

��1����Ӧ���з�Ӧ�Ļ�ѧ����ʽΪ��
��2���������������ʹ�ú�MnO280%���ϵĸ�����ΪMnO2������͵�ƶ����Al��Si�������ﺬ���ϸߣ��ᵼ��KOH������
��3�������������ĵ缫��Ӧ����ʽΪ��
��4���ڴ�ͳ�����еõ�K2MnO4��������ͨ��CO2�Ʊ�KMnO4����ѧ��Ӧ����ʽΪ��3K2MnO4+2CO2�T2KMnO4+MnO2+2K2CO3 ����������Ӧ����MnԪ�صĽǶȿ���KMnO4�IJ������Ϊ
��5���ⶨ���������Ʒ���ȵķ����ǣ�����������Һ�еμ���������Һ������ɫ��������Ӧ�����ӷ���ʽ
��6����֪������KSP��Mn��OH��2��=2.0��10-23����ҵ�ϵ���PH������ˮ�е�Mn2+����pH=10ʱ��c��Mn2+��=
���㣺���ԭ��,���ܵ���ʵ��ܽ�ƽ�⼰����ת���ı���
ר�⣺����ƽ������Һ��pHר��,�绯ѧר��
��������1����������������������MnO2�õ�K2MnO4��д����Ӧ�ķ���ʽ��
��2��������������������������ܺ�ǿ�Ӧ����ƫ�����κ�ˮ�����Իᵼ��KOH������ƫ�ߣ�
��3���ڵ������ò������������������������K2MnO4��Һ�õ�KMnO4��������ˮ�õ��ӷ�����ԭ��Ӧ�������������������ӣ����������������ʧ���ӷ�Ӧ������Ӧ���ɸ���������ӣ�
��4�����ݻ�ѧ��Ӧ����ʽΪ��3K2MnO4+2CO2�T2KMnO4+MnO2+2K2CO3����KMnO4�IJ��ʣ���ⷨ����������KMnO4�����ʸ��ߣ�
��5������������ԭ��Ӧԭ����д��
��6����֪������KSP��Mn��OH��2��=c��Mn2+����c��OH-��2���pH=10����c��Mn2+����
��2��������������������������ܺ�ǿ�Ӧ����ƫ�����κ�ˮ�����Իᵼ��KOH������ƫ�ߣ�
��3���ڵ������ò������������������������K2MnO4��Һ�õ�KMnO4��������ˮ�õ��ӷ�����ԭ��Ӧ�������������������ӣ����������������ʧ���ӷ�Ӧ������Ӧ���ɸ���������ӣ�
��4�����ݻ�ѧ��Ӧ����ʽΪ��3K2MnO4+2CO2�T2KMnO4+MnO2+2K2CO3����KMnO4�IJ��ʣ���ⷨ����������KMnO4�����ʸ��ߣ�
��5������������ԭ��Ӧԭ����д��
��6����֪������KSP��Mn��OH��2��=c��Mn2+����c��OH-��2���pH=10����c��Mn2+����
���
�⣺��1���������̺��������ء�����������������غ�ˮ����Ӧ�Ļ�ѧ����ʽΪ4KOH+2MnO2+O2=2K2MnO4+2H2O��
�ʴ�Ϊ��4KOH+2MnO2+O2=2K2MnO4+2H2O��
��2�������������������������ǿ�ᷴӦҲ����ǿ�Ӧ��������������ǿ�Ӧ����ƫ�����κ�ˮ����Ӧ�Ļ�ѧ����ʽΪ2KOH+Al2O3=2KAlO2+H2O�����Իᵼ��KOH������ƫ�ߣ��ʴ�Ϊ��ƫ�ߣ�2KOH+Al2O3=2KAlO2+H2O��
��3������������Һʱ��������ˮ�õ����������������������ӣ��缫��ӦΪ2H2O+2e-=H2��+2OH-�����������������ʧ�������ɸ���������ӣ��缫��ӦʽΪ2MnO42--2e-=2MnO4-���ʴ�Ϊ��2MnO42--2e-=2MnO4-��
��4���ɻ�ѧ��Ӧ����ʽΪ��3K2MnO4+2CO2�T2KMnO4+MnO2+2K2CO3�����ó���3���̲μӷ�Ӧ����2��KMnO4������KMnO4�IJ������Ϊ
��100%=66.7%����ô�ͳ������ȣ���ⷨ����������KMnO4�����ʸ��ߣ����������Dz��ʸ��ߡ�KOHѭ�����ã��ʴ�Ϊ��66.7%�����ʸ��ߡ�KOHѭ�����ã�
��5������������Һ�еμ���������Һ������ɫ����������������ԭ��Ӧ���ϼ��������н������ɫ����Ϊ�������̣����Է�Ӧ�����ӷ���ʽ3Mn2++2MnO4-+2H2O=5MnO2��+4H+���ʴ�Ϊ��3Mn2++2MnO4-+2H2O=5MnO2��+4H+��
��6����֪������KSP��Mn��OH��2��=c��Mn2+����c��OH-��2��=2.0��10-23����pH=10������c��OH-��=10-4mol/L������c��Mn2+��=
=2��10-15mol/L���ʴ�Ϊ��2��10-15��
�ʴ�Ϊ��4KOH+2MnO2+O2=2K2MnO4+2H2O��
��2�������������������������ǿ�ᷴӦҲ����ǿ�Ӧ��������������ǿ�Ӧ����ƫ�����κ�ˮ����Ӧ�Ļ�ѧ����ʽΪ2KOH+Al2O3=2KAlO2+H2O�����Իᵼ��KOH������ƫ�ߣ��ʴ�Ϊ��ƫ�ߣ�2KOH+Al2O3=2KAlO2+H2O��
��3������������Һʱ��������ˮ�õ����������������������ӣ��缫��ӦΪ2H2O+2e-=H2��+2OH-�����������������ʧ�������ɸ���������ӣ��缫��ӦʽΪ2MnO42--2e-=2MnO4-���ʴ�Ϊ��2MnO42--2e-=2MnO4-��
��4���ɻ�ѧ��Ӧ����ʽΪ��3K2MnO4+2CO2�T2KMnO4+MnO2+2K2CO3�����ó���3���̲μӷ�Ӧ����2��KMnO4������KMnO4�IJ������Ϊ
| 2 |
| 3 |
��5������������Һ�еμ���������Һ������ɫ����������������ԭ��Ӧ���ϼ��������н������ɫ����Ϊ�������̣����Է�Ӧ�����ӷ���ʽ3Mn2++2MnO4-+2H2O=5MnO2��+4H+���ʴ�Ϊ��3Mn2++2MnO4-+2H2O=5MnO2��+4H+��
��6����֪������KSP��Mn��OH��2��=c��Mn2+����c��OH-��2��=2.0��10-23����pH=10������c��OH-��=10-4mol/L������c��Mn2+��=
| 2.0��10 -23 |
| (10 -4) 2 |
�����������Ե��ԭ��Ϊ���忼���˵缫��Ӧʽ����д����ѧ��Ӧ����ʽ����д��֪ʶ�㣬�ѶȲ������������֪����ȷ�������ﲢд����Ӧ����ʽ�ǽⱾ��Ĺؼ���

��ϰ��ϵ�д�
�����Ŀ
0.03molCu��ȫ�������ᣬ�������������NO��NO2��N2O4��������干0.05mol���û�������ƽ����Է������������ǣ�������
| A��30 | B��46 | C��50 | D��66 |
��Cu��OH��2��������Ӿʵ��ʱ������������ɫ������˽����м�����������ʱ�����������۵��ǣ�������
| A����ˮ | B�����ú����ˮ |
| C�������������� | D����������Һ |
ͬ��ͬѹ�£���������SO2��CO2��Ƚϣ�����������ȷ���ǣ�������
| A���ܶȱ�Ϊ16��11 |
| B���ܶȱ�Ϊ11��16 |
| C�������Ϊ1��1 |
| D�������Ϊ11��16 |
�����£�pH��ͬ�����ͬ�Ĵ��������������Һ�ֱ��ȡ���д�ʩ���й�������ȷ���ǣ�������
| A����ˮϡ��2��������Һ��pH����С |
| B��ʹ�¶ȶ�����20�������Һ��pH������ |
| C���������Ĵ����ƾ��������Һ��pH������ |
| D����������п��ַ�Ӧ��������������������� |
��0.1mol?L-1��CH3COOH��Һ�д������µ���ƽ��CH3COOH?CH3COO-+H+ ���ڸ�ƽ�⣬����������ȷ���ǣ�������
| A���������������ᣬ��Һ��pH��С��CH3COOH�ĵ�������� | ||
| B���μ�����0.1mol/LHCl��Һ����Һ��C��H+������ | ||
| C����������Na2CO3���壬ƽ�ⲻ�ƶ� | ||
D����ˮϡ�ͣ���ʹ��Һ��
|
һ���¶��£���0.1mol HI����1Lij�ܱ���ƿ�з�����Ӧ��2HI��g��?H2��g��+I2��g�������н��۲���˵��������Ӧ�ﵽƽ��״̬���ǣ�������
| A����ƿ���������ɫ���ټ��� |
| B��HI������������H2����������֮��Ϊ2��1 |
| C��I2������������I2������������� |
| D����ƿ��������������� |
 �������ڲ�ͬ�ܼ�����NaOH������ͬ���͵ķ�Ӧ�����ɲ�ͬ�ķ�Ӧ�����������������ʣ������������̽����
�������ڲ�ͬ�ܼ�����NaOH������ͬ���͵ķ�Ӧ�����ɲ�ͬ�ķ�Ӧ�����������������ʣ������������̽����