题目内容
已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素,B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.请回答下列问题:
(1)B、C、D三种元素的电负性由大到小的顺序是 (填元素符号).
(2)在A元素与上述其他元素形成的分子中,其中心原子为sp3杂化的分子式为 (写出2种即)
(3)与C同族、且位于第四周期元素所形成气态化物的电子式为 ,它属于 (填“极性”或“非极性”)分子,其沸点低于C的氢化物的沸点,主要原因是 .
(4)F的基态原子核外电子排布式是 .
(5)E原子的第一电离能比同周期后面相邻元素的第一电离能 (填“大”或“小”).
(1)B、C、D三种元素的电负性由大到小的顺序是
(2)在A元素与上述其他元素形成的分子中,其中心原子为sp3杂化的分子式为
(3)与C同族、且位于第四周期元素所形成气态化物的电子式为
(4)F的基态原子核外电子排布式是
(5)E原子的第一电离能比同周期后面相邻元素的第一电离能
考点:位置结构性质的相互关系应用
专题:
分析:根据A是周期表中原子半径最小的元素,所以A为:H;
根据B的基态原子有3个不同的能级,各能级中电子数相等得出B是1s2 2s2 2p2,故B为:C;
根据D的基态原子2p能级上的未成对电子数与B原子相同,故D为:O;
依据A、B、C、D、E原子序数逐渐增大,可知C为:N;
D2-离子与E2+离子具有相同的稳定电子层结构,则E是Mg.
F4+离子和氩原子的核外电子排布相同,则F为22号元素:Ti;
X的基态原子的外围电子排布式为3d84s2,则X是Ni,据此解答各小题即可.
根据B的基态原子有3个不同的能级,各能级中电子数相等得出B是1s2 2s2 2p2,故B为:C;
根据D的基态原子2p能级上的未成对电子数与B原子相同,故D为:O;
依据A、B、C、D、E原子序数逐渐增大,可知C为:N;
D2-离子与E2+离子具有相同的稳定电子层结构,则E是Mg.
F4+离子和氩原子的核外电子排布相同,则F为22号元素:Ti;
X的基态原子的外围电子排布式为3d84s2,则X是Ni,据此解答各小题即可.
解答:
解:依据分析可知:A为氢,B为碳,C为氮,D为氧,E为镁,F为钛,X为镍,
(1)C、N、O为同一周期元素,同周期从左到右电负性依次增强,所以O>N>C,
故答案为:O>N>C;
(2)中心原子通过sp3杂化形成分子,则说明中心原子含有4个价电子对,价层电子对数=σ 键个数+
(a-xb),则CH4、H2O都含有4个价电子对,
故答案为:CH4、H2O;
(3)与氮元素同主族的第四周期元素是As,AsH3,电子式为; ,其氢化物为其结构与氨气相似,所以其氢化物是极性分子,由于NH3分子中存在氢键,而AsH3中不存在氢键,故AsH3的沸点低于NH3,
,其氢化物为其结构与氨气相似,所以其氢化物是极性分子,由于NH3分子中存在氢键,而AsH3中不存在氢键,故AsH3的沸点低于NH3,
故答案为: ;极性;NH3分子中存在氢键,而AsH3中不存在氢键;
;极性;NH3分子中存在氢键,而AsH3中不存在氢键;
(4)F为22号元素:Ti,其核外有22个电子,电子排布式为1s22s22p63s23p63d24s2,故答案为:1s22s22p63s23p63d24s2;
(5)Mg的最外层电子排布为3s2,属于能量最低的全排满结构,不易失去电子,所以第一电离能大,
故答案为:大.
(1)C、N、O为同一周期元素,同周期从左到右电负性依次增强,所以O>N>C,
故答案为:O>N>C;
(2)中心原子通过sp3杂化形成分子,则说明中心原子含有4个价电子对,价层电子对数=σ 键个数+
| 1 |
| 2 |
故答案为:CH4、H2O;
(3)与氮元素同主族的第四周期元素是As,AsH3,电子式为;
 ,其氢化物为其结构与氨气相似,所以其氢化物是极性分子,由于NH3分子中存在氢键,而AsH3中不存在氢键,故AsH3的沸点低于NH3,
,其氢化物为其结构与氨气相似,所以其氢化物是极性分子,由于NH3分子中存在氢键,而AsH3中不存在氢键,故AsH3的沸点低于NH3,故答案为:
 ;极性;NH3分子中存在氢键,而AsH3中不存在氢键;
;极性;NH3分子中存在氢键,而AsH3中不存在氢键;(4)F为22号元素:Ti,其核外有22个电子,电子排布式为1s22s22p63s23p63d24s2,故答案为:1s22s22p63s23p63d24s2;
(5)Mg的最外层电子排布为3s2,属于能量最低的全排满结构,不易失去电子,所以第一电离能大,
故答案为:大.
点评:本题考查了物质结构推断题,利用电子排布的有关知识加以推断,难度较大.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
下列电离方程式错误的是( )
| A、NaHSO4═Na++H++SO42- |
| B、NaHCO3═Na++H++CO32- |
| C、MgCl2═Mg2++2Cl- |
| D、Ba(OH)2═Ba2++2OH- |
下列各组有机物中,只用一种试剂无法鉴别的是( )
| A、苯、苯酚、己烯 |
| B、苯、甲苯、乙苯 |
| C、乙醇、甲苯、硝基苯 |
| D、乙醇、乙醛、乙酸 |
液化石油气的主要成分为丙烷和丁烷,下列有关说法错误的是( )
| A、丙烷和丁烷均属于烷烃 |
| B、两者分子中均含有碳碳双键 |
| C、丙烷和丁烷燃烧均是放热反应 |
| D、丙烷和丁烷充分燃烧均生成二氧化碳和水 |
下列卤代烃中,既能发生取代反应又能发生消去反应的是( )
| A、CH3Cl |
| B、CH3CH2CH2Br |
C、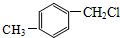 |
D、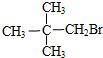 |
某溶液可能含有Clˉ、SO42-、CO32-、NH4+、Fe3+、Al3+、AlO2-和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中A( )
| A、至少存在4种离子 |
| B、Clˉ一定存在,且c(Clˉ)=0.4mol?L-1 |
| C、SO42ˉ、NH4+一定存在,AlO2-可能存在 |
| D、CO32ˉ、Al3+一定不存在,K+可能存在 |
下列除杂质的方法错误的是( )
| 物质(括号内为杂质) | 除杂方法 | |
| A | CO2(O2) | 灼热的铜网 |
| B | FeCl2溶液(CuCl2) | 加入过量铁粉,过滤 |
| C | CaCl2溶液(盐酸) | 加入过量CaCO3,过滤 |
| D | CO2(CO) | 通入O2 点燃 |
| A、A | B、B | C、C | D、D |
下列热化学方程式书写正确的是(△H的绝对值均正确)( )
| A、C(s)+O2(g)=CO2(g);△H=-315kJ |
| B、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.3kJ?mol-1 |
| C、C2H5OH+3O2=2CO2+3H2O;△H=-1368.8kJ?mol-1 |
| D、2H2O(g)=2H2(g)+O2(g);△H=-483.6kJ?mol-1 |