题目内容
7.下列推断合理的是( )| A. | 铜与浓硝酸反应时,硝酸既表现氧化性又表现酸性 | |
| B. | 金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 | |
| C. | 浓H2SO4有强氧化性,常温下能与Cu发生剧烈反应 | |
| D. | 将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入氯水,氯水褪色后加热也能恢复原色 |
分析 A.铜和浓硝酸反应时生成二氧化氮和硝酸铜,部分N元素化合价降低、部分N元素化合价不变;
B.金刚石是碳元素的一种同素异形体,碳单质都可以和氧气之间反应;
C.浓硫酸在常温下与铜不反应;
D.二氧化硫的漂白性具有不稳定性,二氧化硫具有还原性和氯气发生氧化还原反应;
解答 解:A.铜和浓硝酸反应时生成二氧化氮和硝酸铜,部分N元素化合价降低、部分N元素化合价不变,所以硝酸体现氧化性和酸性,故A正确;
B.金刚石的硬度很大,能与足量氧气发生反应生成二氧化碳,故B错误;
C.浓硫酸在常温下与铜不反应,只在加热条件下反应,故C错误;
D.二氧化硫的漂白性具有不稳定性,二氧化硫和氯气发生氧化还原反应生成硫酸和盐酸,氯水褪色后加热也不能恢复原色,故D错误;
故选A.
点评 本题考查较为综合,涉及元素化合物知识的综合理解和运用,有利于培养学生的良好科学素养和提高学习的积极性,难度不大,注意相关基础知识的积累和学习.

练习册系列答案
相关题目
19.在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
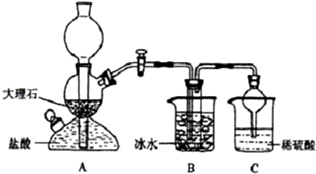
(1)A装置中所发生反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O.C装置中稀硫酸的作用为:吸收从B装置中的试管内逸出的氨气,减少对环境的污染.
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
参照表中数据,请分析B装置中使用冰水是因为温度越低碳酸氢钠溶解度越小,便于析出.
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在AB装置之间(填写字母)连接一个盛有饱和碳酸氢钠溶液 的洗气装置,其作用是除去二氧化碳气体中的氯化氢气体.
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为60%.

(1)A装置中所发生反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O.C装置中稀硫酸的作用为:吸收从B装置中的试管内逸出的氨气,减少对环境的污染.
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在AB装置之间(填写字母)连接一个盛有饱和碳酸氢钠溶液 的洗气装置,其作用是除去二氧化碳气体中的氯化氢气体.
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为60%.
18.两电极用导线连接插入电解质溶液中(不考虑溶液中溶解的氧气的影响),你认为不能构成原电池的是( )
| 选项 | A | B | C | D |
| 电极材料 | Zn | Fe | Cu | Al |
| 电极材料 | Cu | Zn | Ag | C |
| 电解质溶液 | CuCl2溶液 | H2SO4溶液 | CuSO4溶液 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
15.下列关于有机物的说法错误的是( )
| A. | CCl4可由CH4制得,可萃取碘水中的碘 | |
| B. | 苯酚钠溶液中通入CO2生成苯酚,则碳酸的酸性比苯酚强 | |
| C. | 乙醇、乙醛和溴乙烷可以用银氨溶液鉴别 | |
| D. | 苯不能使酸性KMnO4溶液褪色,因此苯不能发生氧化反应 |
2.以下物质既能使酸性KMnO4溶液褪色,又能使溴水因发生化学反应而褪色的是( )
①甲醛②苯③聚乙烯④聚乙炔⑤2-丁炔⑥环己烷⑦邻二甲苯⑧苯乙烯.
①甲醛②苯③聚乙烯④聚乙炔⑤2-丁炔⑥环己烷⑦邻二甲苯⑧苯乙烯.
| A. | ①④⑤⑧ | B. | ④⑤⑦⑧ | C. | ①③④⑤ | D. | ③④⑤⑦⑧ |
12.某炔烃与氢气加成得到2-甲基-3-乙基戊烷,该炔烃可能的结构有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
19.下列结论不正确的是( )
| A. | 微粒半径:K+>Al3+>S2->Cl- | B. | 离子的还原性:Cl-<Br-<I- | ||
| C. | 酸性:H2SO4>H3PO4>H2CO3 | D. | 金属性:K>Ca>Mg>Be |
16.有关下列微粒的化学用语正确的是( )
| A. | CS2的电子式为: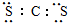 | B. | Ca2+的离子结构示意图为: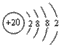 | ||
| C. | HClO的结构式为:H-O-Cl | D. | 氯化铵的电子式为: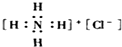 |
17.下列关于化学用语的表示正确的是( )
| A. | 乙烯的结构简式:CH2 CH2 | |
| B. | 硫离子结构示意图: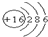 | |
| C. | CaF2的电子式: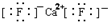 | |
| D. | 硫酸铁的电离方程式:Fe2(SO4)3=Fe23++3SO42- |