题目内容
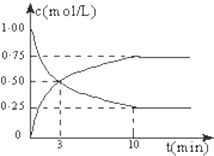 在体积恒定的密闭容器中,充入2mol CO2和5mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示:
在体积恒定的密闭容器中,充入2mol CO2和5mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示:(1)从反应开始到第10min,H2的转化率为
a.向正向移动 b.向逆向移动
c.不移动 d.无法确定平衡移动方向
(2)下列措施中能使
| n(CH3OH) |
| n(CO2) |
a.升高温度 b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离 d.再充入l mol CH3OH(g)
考点:化学平衡的计算,化学平衡的影响因素
专题:化学平衡专题
分析:(1)由图象可知v(CO2),根据反应速率之比等于化学计量数之比计算氢气的反应速率,计算出平衡时各物质的浓度,根据平衡常数表达式计算,结合浓度商和平衡常数比较判断反应进行的方向;
(2)为使甲醇与二氧化碳的物质的量比值增大,应使平衡向正反应方向移动,或增加甲醇的物质的量.
(2)为使甲醇与二氧化碳的物质的量比值增大,应使平衡向正反应方向移动,或增加甲醇的物质的量.
解答:
解:(1)由图象可知,二氧化碳起始浓度为1mol/L,则体积为2L,在这段时间内,反应消耗的CO2为2L×0.75mol/L=1.5mol,消耗氢气物质的量=3×1.5mol=4.5mol;则氢气转化率=
×100%=90%,
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始:2mol 5mol 0 0
转化:1.5mol 4.5mol 1.5mol 1.5mol
平衡:0.5mol 0.5mol 1.5mol 1.5mol
所以:达到平衡时,c(CO2)=0.25mol/L,c(H2)=0.25mol/L,c(CH3OH)=0.75mol/L,c(H2O)=0.75mol/L,
在该条件下,反应的平衡常数K的值=
=144,只改变浓度,使c(CO2)=1.00mol/L,c(H2)=0.40mol/L,c(CH3OH)=c(H2O)=0.80mol/L,
则此时Qc=
=10<K,则平衡向正反应方向移动,故选a;
故答案为:90%;144;a;
(2)a、升高温度,平衡向逆反应方向移动,甲醇与二氧化碳的物质的量比值减小,故a错误;
b、充入He(g),使体系压强增大,但对反应物质没有影响,平衡不移动,二者比值不变,故b错误;
c、将H2O(g)从体系中分离,生成物的浓度减小,平衡向正反应方向移动,二者比值变大,故c正确;
d、再充入l mol CH3OH(g),反应虽然向逆反应方向移动,但反应的比增加的少,二者比值增大,故d正确.
故答案为:cd.
| 4,5mol |
| 5mol |
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始:2mol 5mol 0 0
转化:1.5mol 4.5mol 1.5mol 1.5mol
平衡:0.5mol 0.5mol 1.5mol 1.5mol
所以:达到平衡时,c(CO2)=0.25mol/L,c(H2)=0.25mol/L,c(CH3OH)=0.75mol/L,c(H2O)=0.75mol/L,
在该条件下,反应的平衡常数K的值=
| 0.75×0.75 |
| 0.25×0.253 |
则此时Qc=
| 0.8×0.8 |
| 1×0.43 |
故答案为:90%;144;a;
(2)a、升高温度,平衡向逆反应方向移动,甲醇与二氧化碳的物质的量比值减小,故a错误;
b、充入He(g),使体系压强增大,但对反应物质没有影响,平衡不移动,二者比值不变,故b错误;
c、将H2O(g)从体系中分离,生成物的浓度减小,平衡向正反应方向移动,二者比值变大,故c正确;
d、再充入l mol CH3OH(g),反应虽然向逆反应方向移动,但反应的比增加的少,二者比值增大,故d正确.
故答案为:cd.
点评:本题考查化学平衡的有关计算,本题难度不大,做题时注意平衡常数的计算和应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列离子组能大量共存的是( )
| A、Ba2+、Cl-、SO42-、K+ |
| B、Mg2+、SO42-、Na+、Cl- |
| C、H+、CO32-、Al3+、Cl- |
| D、K+、Fe2+、NO3-、H+ |
在1L密闭容器发生反应:4NH3(g)+5O2(g)?4NO(g)+6HO(g)△H=-Q kJ?mol-1(Q>0),容器内部分物质的物质的量浓度如下表:
下列说法错误的是( )
| 时间/浓度 | c(NH3)(mol?L-1) | c(O2)(mol?L-1) | c(NO)(mol?L-1) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.7 | 1.475 | 0.1 |
| 第10min | 0.7 | 1.475 | 0.1 |
| A、反应在第2min到第4min时,O2的平均速率为0.1875mol?L-1?min-1 |
| B、反应在第2min时改变了某一条件,该条件可能是使用催化剂或升高温度 |
| C、第4min、第8min时分别达到化学平衡,且平衡常数相同 |
| D、在开始反应的前2min内,该反应放出0.05QKJ的热量 |
下列各组分子中,都属于含极性键的非极性分子的是( )
| A、CO2 H2S |
| B、C60 C2H4 |
| C、C2H4 CH4 |
| D、NH3 HCl |