题目内容
含有极性键的共价化合物是( )
| A、Na2O2 |
| B、NaOH |
| C、H2 |
| D、HCl |
考点:极性键和非极性键,共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:化合物中至少含有两种元素,共价化合物中不含离子键,同种非金属元素之间以非极性键相结合,不同非金属元素之间以极性键相结合,据此解答.
解答:
解:A.Na2O2是钠离子和过氧根离子构成的离子化合物,电子式为 ,含有离子键和非极性键,属于含有非极性键的离子化合物,故A错误;
,含有离子键和非极性键,属于含有非极性键的离子化合物,故A错误;
B.NaOH含有离子键和极性键,电子式为: ,为离子化合物,故B错误;
,为离子化合物,故B错误;
C.H2中只含有非极性共价键,属于单质,故C错误;
D.HCl中只含C-Cl极性共价键,属于共价化合物,故D正确;
故选D.
 ,含有离子键和非极性键,属于含有非极性键的离子化合物,故A错误;
,含有离子键和非极性键,属于含有非极性键的离子化合物,故A错误;B.NaOH含有离子键和极性键,电子式为:
 ,为离子化合物,故B错误;
,为离子化合物,故B错误;C.H2中只含有非极性共价键,属于单质,故C错误;
D.HCl中只含C-Cl极性共价键,属于共价化合物,故D正确;
故选D.
点评:本题考查了化学键和化合物的关系,难度不大,注意:离子化合物中可能含有共价键,但共价化合物中一定不含离子键.

练习册系列答案
相关题目
对于某一可逆反应,在不同条件下的平衡状态中,正、逆反应速率的关系是( )
A、 |
B、 |
C、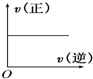 |
D、 |
向某NaOH溶液中通人CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示四种情况,且(2)、(3)、(4)图中分别有OA<AB,OA=AB,OA>AB,则下列分析与判断不正确的是( )(不计CO2的溶解)


| A、M中只有一种溶质的有(1)和(3) |
| B、M中有两种溶质的有(2)和(4) |
| C、(3)图显示M的溶质为Na2CO3 |
| D、(4)图显示M的溶质为NaHCO3和 Na2CO3 |
自然界中存在一种尖晶石,主要成分的化学式可表示为MgA12O4,可作为宝石.已知该尖晶石中混有Fe2O3.取5.4g样品,恰好完全溶解在100mL一定浓度的盐酸中,则该盐酸的浓度可能是( )
| A、1.8mol/L |
| B、2.8mol/L |
| C、4.3mol/L |
| D、4.9mol/L |
各0.9879g 24℃、101.325kpa下的下列物质,所占体积最小的是( )
| A、O2 |
| B、H2 |
| C、Cl2 |
| D、CuO |
下列10种物质:①苯甲酸②苯酚③乙酸④乙酸乙酯⑤羟基乙酸⑥甲醛 ⑦溴水⑧NaOH溶液⑨钠⑩FeCl3溶液.前五种物质中的一种能与后五种物质反应,后五种物质中的一种能与前五种物质反应,这两种物质是( )
| A、③⑧ | B、②⑧ | C、②⑦ | D、⑤⑨ |
下列说法不正确的是( )
| A、麦芽糖及其水解产物均能与新制氢氧化铜悬浊液反应 |
| B、用溴水即可鉴别苯酚溶液、2,4-已二烯和甲苯 |
| C、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
D、甘氨酸与盐酸反应的化学方程式为: +HCl→ +HCl→ |
 锌银电池能量大、电压平稳,广泛用于电子手表、照相机、计算器和其他微型电子仪器.电解质溶液是KOH溶液,电池总反应为Zn+Ag2O═ZnO+2Ag.请回答下列问题:
锌银电池能量大、电压平稳,广泛用于电子手表、照相机、计算器和其他微型电子仪器.电解质溶液是KOH溶液,电池总反应为Zn+Ag2O═ZnO+2Ag.请回答下列问题: