题目内容
 按要求回答下列问题
按要求回答下列问题(1)石墨晶体中C-C键的键角为
(2)金刚石晶体中含有共价键形成的C原子环,其中最小的C环上有
(3)CsCl晶体中每个Cs+周围有
(4)白磷分子中的键角为
(5)二氧化硅是一种
(6)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体.其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答.这个基本结构单元由
考点:晶胞的计算
专题:化学键与晶体结构
分析:(1)根据石墨晶体的结构判断;
(2)根据金刚石晶胞结构判断;
(3)根据CsCl晶体的晶胞分析;
(4)根据白磷分子的空间构型判断含有的共价键数目;白磷含有6个共价键,可形成化合物P4O10;
(5)根据二氧化硅组成微粒判断晶体类型;根据晶体结构判断氧原子数;
(6)根据晶体硼的晶胞结构判断.
(2)根据金刚石晶胞结构判断;
(3)根据CsCl晶体的晶胞分析;
(4)根据白磷分子的空间构型判断含有的共价键数目;白磷含有6个共价键,可形成化合物P4O10;
(5)根据二氧化硅组成微粒判断晶体类型;根据晶体结构判断氧原子数;
(6)根据晶体硼的晶胞结构判断.
解答:
解:(1)石墨片层内形成正六边形,键角为120°;每个六边形含有6个碳原子,每个碳原子被3个六边形共有,则每个六边形含有6×
=2,
故答案为:120°;2;
(2)金刚石晶体中6个碳原子构成一个碳环,每个C原子被12个最小环所共用;平均每个最小环含6×
=
个C原子,
故答案为:
;
(3)CsCl晶体中每个Cs+周围紧邻的有8个Cl-,每个Cs+周围与它最近且距离相等的Cs+共有6个;
故答案为:8;6;
(4)白磷为正四面体结构,所以键角为60°,每个P原子与3个P原子结合成共价键,每个分子中含有6个共价键,若将1分子白磷中的所有P-P键打开并各插入一个氧原子,共可结合6个O原子,若每个P原子上的孤对电子分别再以配位键连接一个氧原子,还可结合4个O原子,则可形成化合物P4O10,
故答案为:60°;正四面体;3;6;P4O10;
(5)二氧化硅有氧原子和硅原子组成,属于原子晶体;晶体微观结构为网状结构,每个Si原子上连接4个氧原子,每个氧原子上连接2个硅原子(就相当于金刚石网状结构中每个Si-Si键之间插入一个氧原子),
故答案为:原子;4;
(6)硼原子组成的正二十面体,即每个面就是一个等边三角形,共有20个面,每个顶点为5个三角形所共用,所以20个等边三角形所含有的顶角数=20×3÷5=12,即原子个数为12;因为每条边为2个三角形所共用,所以20个等边三角形含有的边数=20×3÷2=30,即B-B键数为30,
故答案为:12;30.
| 1 |
| 3 |
故答案为:120°;2;
(2)金刚石晶体中6个碳原子构成一个碳环,每个C原子被12个最小环所共用;平均每个最小环含6×
| 1 |
| 12 |
| 1 |
| 2 |
故答案为:
| 1 |
| 2 |
(3)CsCl晶体中每个Cs+周围紧邻的有8个Cl-,每个Cs+周围与它最近且距离相等的Cs+共有6个;
故答案为:8;6;
(4)白磷为正四面体结构,所以键角为60°,每个P原子与3个P原子结合成共价键,每个分子中含有6个共价键,若将1分子白磷中的所有P-P键打开并各插入一个氧原子,共可结合6个O原子,若每个P原子上的孤对电子分别再以配位键连接一个氧原子,还可结合4个O原子,则可形成化合物P4O10,
故答案为:60°;正四面体;3;6;P4O10;
(5)二氧化硅有氧原子和硅原子组成,属于原子晶体;晶体微观结构为网状结构,每个Si原子上连接4个氧原子,每个氧原子上连接2个硅原子(就相当于金刚石网状结构中每个Si-Si键之间插入一个氧原子),
故答案为:原子;4;
(6)硼原子组成的正二十面体,即每个面就是一个等边三角形,共有20个面,每个顶点为5个三角形所共用,所以20个等边三角形所含有的顶角数=20×3÷5=12,即原子个数为12;因为每条边为2个三角形所共用,所以20个等边三角形含有的边数=20×3÷2=30,即B-B键数为30,
故答案为:12;30.
点评:本题考查了晶体的结构分析,掌握常见晶胞的结构是解题的关键,题目难度中等.

练习册系列答案
相关题目
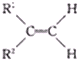 +
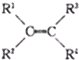
+
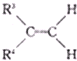 +
+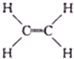 ,其实质是
,其实质是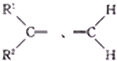 等)卡宾再结合生成烯烃,则分子式为C4H8和C5H10的混合烯烃发生该发生该类反应,则新生成的有机物最多有( )
等)卡宾再结合生成烯烃,则分子式为C4H8和C5H10的混合烯烃发生该发生该类反应,则新生成的有机物最多有( )