题目内容
分别用一种化学药品将下列溶液中混入的少量杂质除去(括号内为杂质)
| 物质 | 需加入的药品 | 离子方程式 |
| CaCl2( CaCO3) | ||
| FeSO4 (CuSO4) | ||
| Cu(Al) |
考点:物质的检验和鉴别的实验方案设计,离子方程式的书写
专题:离子反应专题
分析:CaCO3可与盐酸反应生成CaCl2;
Fe可置换出铜;
Al可与盐酸反应.
Fe可置换出铜;
Al可与盐酸反应.
解答:
解:CaCO3可与盐酸反应生成CaCl2,反应的离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O,
Fe可置换出铜,反应的离子方程式为Fe+Cu2+═Cu+Fe2+;
Al可与盐酸反应的离子方程式为2Al+6H+═2Al3++3H2↑,
故答案为:
Fe可置换出铜,反应的离子方程式为Fe+Cu2+═Cu+Fe2+;
Al可与盐酸反应的离子方程式为2Al+6H+═2Al3++3H2↑,
故答案为:
| 物质 | 需加入的药品 | 离子方程式 |
| CaCl2( CaCO3) | HCl | CaCO3+2H+═Ca2++CO2↑+H2O |
| FeSO4 (CuSO4) | Fe | Fe+Cu2+═Cu+Fe2+ |
| Cu(Al) | HCl | 2Al+6H+═2Al3++3H2↑ |
点评:本题考查物质的分离提纯,为高频考点,侧重物质除杂及混合物分离方法的考查,把握物质的性质及分离原理为解答的关键,题目难度不大,注意把握离子方程式的书写.

练习册系列答案
相关题目
铵盐是一类重要的氮的化合物,设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1 mol NH4+含有的电子数为11N A |
| B、NH4+是正四面体的分子 |
| C、0.1 L 3 mol?L-1的NH4NO3溶液中氮原子数等于0.6N A |
| D、将分子总数为NA的NH3和HCl的混合气体置于标准状况下,其体积约为22.4 L |
下列离子方程式中正确的是( )
| A、H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、金属钠跟水反应:Na+H2O═Na++OH-+H2↑ |
| C、澄清的石灰水跟盐酸反应:H++OH-═H2O |
| D、氯气与水反应Cl2+H2O?2H++Cl-+ClO- |
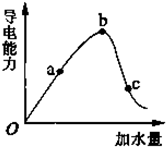 一定温度下,冰醋酸和水稀释过程中溶液的导电能力曲线如图所示,请回答:
一定温度下,冰醋酸和水稀释过程中溶液的导电能力曲线如图所示,请回答: