题目内容
11.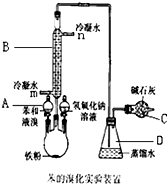 实验室用图装置制取少量溴苯,试填写下列空白.
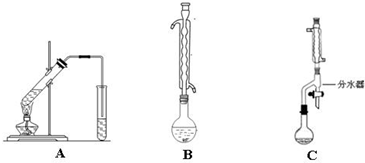
实验室用图装置制取少量溴苯,试填写下列空白.(1)写出仪器A的名称分液漏斗;B的名称冷凝管;
(2)请你写出实验室制取溴苯的化学方程式
 ;
;(3)长导管的下口为什么不插入锥形瓶的液面下防止倒吸
(4)反应完毕后,向烧瓶中滴加NaOH 溶液的作用是:除去溴苯中的溴
(5)冷凝水的进水口是(填m或n)m,图中干燥管C的作用是吸收多余HBr气体,防止空气污染.
分析 (1)熟悉仪器的性质,说出其名称;
(2)液溴与苯在铁做催化剂条件下发生取代反应生成溴苯和溴化氢;
(3)溴化氢易溶于水,容易发生倒吸;
(4)溴与氢氧化钠反应生成溴化钠和次溴酸钠;
(5)根据冷凝效果判断水的流动方向,反应尾气中有挥发的溴和生成的溴化氢,能污染空气,所以要吸收尾气.
解答 解:(1)依据仪器形状可知:A为分液漏斗,B为冷凝管;
故答案为:分液漏斗;冷凝管;
(2)苯与液溴在Fe的催化作用下发生取代反应生成溴苯,其反应的化学方程式为: ;
;
故答案为: .
.
(3)溴化氢易溶于水,容易发生倒吸,长导管的下口不插入锥形瓶可以防止倒吸的发生;
故答案为:防止倒吸;
(4)反应后生成的溴苯中含有少量的溴,溴苯与氢氧化钠不反应,溴与氢氧化钠反应生成溴化钠和次溴酸钠,可用NaOH溶液洗涤除去溴苯中的溴;
故答案为:除去溴苯中的溴;
(5)冷凝水的流动方向应自下而上,这样的冷却效果好,确保充分冷却,反应尾气中有挥发的溴和生成的溴化氢,能污染空气,所以要用碱石灰吸收尾气,
故答案为:m;吸收多余HBr气体,防止空气污染.
点评 本题主要考查了苯的性质实验,掌握反应的原理、各物质的性质以及操作的方法是解题的关键,难度不大.

练习册系列答案
相关题目
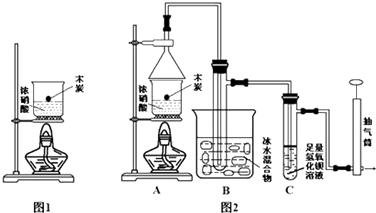
19.三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物.探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,Cu2O在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则实验现象是固体完全溶解,溶液呈血红色.
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?不合理;当原固体粉末为Fe2O3和Cu2O的混合物时,加入稀H2SO4后产生的Fe3+与Cu反应生成Fe2+,滴加KSCN溶液后也可能不变红色.
(3)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明原固体粉末是Fe2O3和Cu2O,写出发生反应的离子方程式Cu2O+2H+═Cu+Cu2++H2O、2Fe3++Cu═2Fe2++Cu2+.
探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为$\frac{9(b-a)}{a}$×100%.
(5)欲利用红色粉末Fe2O3和Cu2O的混合物制取较纯净的胆矾 (CuSO4•5H2O)经查阅资料得知,在溶液中调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH
实验室有下列试剂可供选择:
A.氯水 B.H2O2 C.硝酸 D.NaOH E.氨水 F.Cu2(OH)2CO3
实验小组设计如下实验方案:
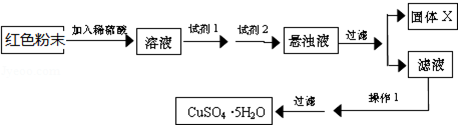
试回答:①试剂I为B,试剂II为F(填字母).
②固体X的化学式为Fe(OH)3.
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,Cu2O在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则实验现象是固体完全溶解,溶液呈血红色.
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?不合理;当原固体粉末为Fe2O3和Cu2O的混合物时,加入稀H2SO4后产生的Fe3+与Cu反应生成Fe2+,滴加KSCN溶液后也可能不变红色.
(3)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明原固体粉末是Fe2O3和Cu2O,写出发生反应的离子方程式Cu2O+2H+═Cu+Cu2++H2O、2Fe3++Cu═2Fe2++Cu2+.
探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为$\frac{9(b-a)}{a}$×100%.
(5)欲利用红色粉末Fe2O3和Cu2O的混合物制取较纯净的胆矾 (CuSO4•5H2O)经查阅资料得知,在溶液中调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
A.氯水 B.H2O2 C.硝酸 D.NaOH E.氨水 F.Cu2(OH)2CO3
实验小组设计如下实验方案:

试回答:①试剂I为B,试剂II为F(填字母).
②固体X的化学式为Fe(OH)3.
6.某研究小组通过实验探究Cu及其化合物的性质,操作正确且能达到目的是( )
| A. | 将铜丝插入浓硫酸加热,反应后把水加入反应器中,观察硫酸铜溶液的颜色 | |
| B. | 常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成 | |
| C. | 电解CuCl2溶液,若阳极生成11.2L的气体,反应中转移电子为1 mol | |
| D. | 将表面有铜绿的铜器放入盐酸中浸泡,除去铜绿 |
20.下列粒子在化学反应中容易得到电子的是( )
| A. | 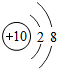 | B. |  | C. | 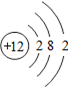 | D. | 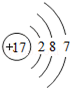 |
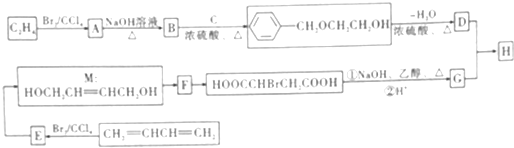
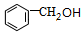 ,F中官能团的名称为羟基、溴原子
,F中官能团的名称为羟基、溴原子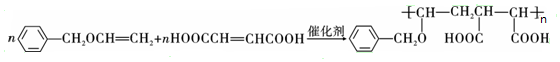
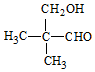 或
或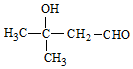 .
.