题目内容
10.将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)═2C(g)若经 2s(秒)后测得 C 的浓度为 0.6mol•L-1,现有下列几种说法正确的是( )①用物质 A 表示的反应的平均速率为 0.3mol•L-1•s-1
②用物质 B 表示的反应的平均速率为 0.6mol•L-1•s-1
③2s 时物质 B 的浓度为 0.7mol•L-1
④2s 时物质 A 的转化率为70%
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ③④ |
分析 将 4mol A 气体和 2mol B 气体在 2L 的密闭容器中混合并在一定条件下发生如下反应 2A(g)+B(g)?2C(g),若经 2s(秒)后测得 C 的浓度为0.6mol•L-1•s-1 ,依据化学平衡三段式列式计算
2A(g)+B(g)?2C(g)
起始量(mol) 4 2 0
变化量(mol) 1.2 0.6 1.2
2s末(mol) 2.8 1.4 2L×0.6mol/L=1.2mol
①用物质A表示反应的平均速率=$\frac{\frac{1.2}{2}}{2}$=0.3mol/L•s;
②用物质B表示反应的平均速率=$\frac{\frac{0.6}{2}}{2}$=0.15mol/L•s;
③2s末物质B的浓度=$\frac{1.4}{2}$=0.7mol•L-1;
④2s末物质A的转化率=$\frac{1.2}{4}$×100%=30%;
解答 解:将 4mol A 气体和 2mol B 气体在 2L 的密闭容器中混合并在一定条件下发生如下反应 2A(g)+B(g)?2C(g),若经 2s(秒)后测得 C 的浓度为0.6mol•L-1•s-1 ,依据化学平衡三段式列式计算
2A(g)+B(g)?2C(g)
起始量(mol) 4 2 0
变化量(mol) 1.2 0.6 1.2
2s末(mol) 2.8 1.4 2L×0.6mol/L=1.2mol
①用物质A表示反应的平均速率=$\frac{\frac{1.2}{2}}{2}$=0.3mol/L•s,故①正确;
②用物质B表示反应的平均速率=$\frac{\frac{0.6}{2}}{2}$=0.15mol/L•s,故②错误;
③2s末物质B的浓度=$\frac{1.4}{2}$=0.7mol•L-1,故③正确;
④2s末物质A的转化率=$\frac{1.2}{4}$×100%=30%,故④错误;
故选A.
点评 本题考查化学平衡三段式计算应用,主要是化学反应速率计算,转化率的计算应用,题目较简单.


平衡移动的因素:①升高温度 ②降低温度 ③增大压强 ④减小压强⑤减小生成物B的浓度 ⑥增加反应物的浓度
平衡移动的方向:①正反应方向移动 ②逆反应方向移动 ③不移动
| 序号 | 平衡移动的因素(填序号) | 平衡移动的方向(填序号) |
| A | ||
| B | ||
| C | ||
| D |
| A. | H2SO4溶液 | B. | BaCl2溶液 | C. | NaOH溶液 | D. | AgNO3溶液 |
| A. | X所形成的单质都是双原子分子 | |
| B. | 原子半径X>Y | |
| C. | X、Y能形成的阴、阳离子数之比为1:2离子化合物,其一定为碱性氧化物 | |
| D. | 由X、Y组成的某化合物与水反应能生成一种强碱和一种弱碱,其简单离子半径:X>Y |
| A. | 除去Fe2O3、Al2O3混合物中的Fe2O3加NaOH溶液 | |
| B. | 除去Na2O2中的Na2O,加热 | |
| C. | 除去Na2CO3固体中的NaHCO3,加NaOH固体 | |
| D. | 除去Fe、C合金中的C,在O2中灼烧 |
①pH=11的氨水bL
②物质的量浓度为1×10-1mol•L-1的氨水cL
③c(OH)=1×10-3mol•L-1的Ba(OH)2溶液dL.
试判断a、b、c、d大小关系正确的为( )
| A. | c>a=d>b | B. | b>a=d>c | C. | c>a>b>d | D. | a=b>c>d |
| A. | NaOH溶液 | B. | AgNO3溶液 | C. | BaCl2溶液 | D. | Ba(OH)2溶液 |
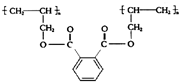 则合成该高聚物的单体的正确组合是( )
则合成该高聚物的单体的正确组合是( )