题目内容
足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A.60 mL B.45 mL C.30 mL D.15 mL
A
【解析】
试题分析:在该反应中Cu失去的电子与硝酸变为各种氮的氧化物得到电子数目相等,各种氮的氧化物在转化为硝酸失去的电子数与氧气得到的电子数目相等。Cu失去电子产生的Cu2+结合的OH-的个数与Cu2+的化合价数目相等。因此n(OH-)=4×(1.68 L÷22.4L/mol)=0.3mol。由于NaOH溶液的浓度是5 mol/L,所以NaOH溶液的体积是V=0.3mol÷5 mol/L=0.06L=60ml。故选项是A。
考点:考查守恒法在氧化还原反应计算中的应用的知识。

练习册系列答案
相关题目
分析下表中各项的排布规律。有机物X是按此规律排布的第19项,下列有关X的组成、性质的说法中肯定错误的是( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
CH4 | CH2O | CH2O2 | CH4O | C2H6 | C2H4O | C2H4O2 | C2H6O |
①是戊酸 ②是戊醇 ③是丁酸甲酯 ④在稀硫酸中易变质 ⑤一定能与钠反应
A.②⑤ B.①③④ C.③④ D.②③⑤

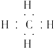
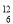 C
C