题目内容
18.设NA代表阿伏加德罗常数的数值,下列说法屮正确的是( )| A. | 标准况状下,44.8 L四氯筑化碳含有的分子数为2NA | |
| B. | 0.1mol/L氯化铝溶液中含有Al3+数为0.1 NA | |
| C. | 1.8 g重水(D2O)中含有的质子数和电子数均为NA | |
| D. | 常温下,O2和O3的混合气体共16g中含有的氧原子数为NA |
分析 A、标况下四氯化碳为液体;
B、溶液体积不明确;
C、重水的摩尔质量为20g/mol;
D、氧气和臭氧均由氧原子构成.
解答 解:A、标况下四氯化碳为液体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、溶液体积不明确,故溶液中的铝离子的个数无法计算,故B错误;
C、重水的摩尔质量为20g/mol,故1.8g重水的物质的量为0.09mol,而重水中含电子和质子书均为10个,故0.09mol重水中含有的质子和中子个数均为0.9NA个,故C错误;
D、氧气和臭氧均由氧原子构成,故16g氧气和臭氧中含有的氧原子的物质的量为1mol,个数为NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意公式的运用和物质的结构特点.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
8.下列关于浓硝酸和浓硫酸的叙述正确的是( )
| A. | 露置在空气中,容器内酸液的质量都减轻 | |
| B. | 常温下都能与铜较快反应 | |
| C. | 常温下都能与氨气反应 | |
| D. | 加热条件下都能与碳反应 |
9.下列叙述正确的是( )
| A. | 铜丝能导电,因此它是电解质 | |
| B. | BaSO4难溶于水,因此它是非电解质 | |
| C. | NaC1熔融状态时能导电,因此它是电解质 | |
| D. | 胶体区别于其他分散系的本质是具有丁达尔效应 |
6.己知:100℃的溫度下,水的离子积Kw=1×10-12.下列说法正确的是( )
| A. | 0.05mol/L 的 H2SO4溶液 PH=1 | |
| B. | 0.001mol/L 的 NaOH溶液 PH=11 | |
| C. | 0.005mol/L的H2SO4溶液与0.0lmol/LNaOH溶液等体积浪合,混合液pH=6,溶液呈酸性 | |
| D. | 完全中和PH=3的H2SO4溶液50mL,需要pH=11的NaOH溶液50mL |
3.化学与生活、社会密切相关.下列说法不正确的是( )
| A. | 制备单晶硅的过程中不发生氧化还原反应 | |
| B. | 绚丽缤纷的烟花中添加了含钾,钙,钠,铜等金属元素化合物 | |
| C. | SiO2、NaOH、HF三者两两均能反应 | |
| D. | 氢氧化铝可作胃酸的中和剂 |
10.如图表示AlCl3溶液与NaOH溶液相互滴加过程中微粒的关系曲线,下列判断正确的是( )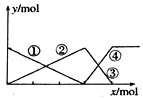

| A. | ①线表示AlO2-的物质的量的变化 | B. | x表示AlCl3的物质的量 | ||
| C. | ③线表示Al(OH)3的物质的量的变化 | D. | ④线表示AlO2-的物质的量的变化 |
1.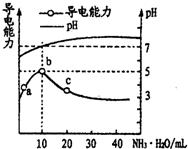 常温下,向10mL0.1mol/L的HR溶液中逐滴滴人0.1mol/L的NH3•H2O溶液,所得溶液pH及导电性变化如图.下列分析正确的是( )
常温下,向10mL0.1mol/L的HR溶液中逐滴滴人0.1mol/L的NH3•H2O溶液,所得溶液pH及导电性变化如图.下列分析正确的是( )
 常温下,向10mL0.1mol/L的HR溶液中逐滴滴人0.1mol/L的NH3•H2O溶液,所得溶液pH及导电性变化如图.下列分析正确的是( )
常温下,向10mL0.1mol/L的HR溶液中逐滴滴人0.1mol/L的NH3•H2O溶液,所得溶液pH及导电性变化如图.下列分析正确的是( )| A. | a→b点导电能力增强,说明HR为弱酸 | |
| B. | b点溶液的pH=5,此时酸碱恰好中和 | |
| C. | c点溶液存在c(OH-)>c(H+) | |
| D. | a、b、c三点NH3•H2O的电离常数均相等 |

