题目内容
6.向FeSO4溶液中滴加少量NaOH溶液时,析出的白色沉淀迅速变为灰绿色,最终变为红褐色.(1)Fe2+离子在水溶液中呈现的颜色是浅绿色;Fe(OH)2转化为红褐色沉淀的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3
(2)有人认为白色沉淀迅速变为灰绿色的原因是Fe(OH)2凝胶吸附了溶液中过量的Fe2+
离子.为探究该观点的正确性,设计如下两个实验:
①向盛有NaOH溶液的试管中加入少量FeS04溶液,若该观点正确,应观察到的现象是析出白色沉淀
②己知胶体粒子的吸附能力随温度升高而下降.向盛装FeSO4溶液的试管中滴加少量NaOH溶液,析出白色沉淀,沉淀迅速变为灰绿色,将此试管小心加热,若观察到灰绿色沉淀变化为白色沉淀,则说明上述解释成立.
分析 (1)亚铁离子在水溶液中呈浅绿色;氢氧化亚铁和空气中氧气、水蒸气反应生成氢氧化铁;
(2)①向盛有NaOH溶液的试管中加入少量FeS04溶液应生成白色沉淀;
②己知胶体粒子的吸附能力随温度升高而下降,升温,吸附的亚铁离子进入溶液,灰绿色沉淀应变化为白色沉淀.
解答 解:(1)亚铁离子在水溶液中呈浅绿色,氢氧化亚铁和空气中氧气、水蒸气反应生成氢氧化铁,反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:浅绿色;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(2)认为白色沉淀迅速变为灰绿色的原因是Fe(OH)2凝胶吸附了溶液中过量的Fe2+离子,
①向盛有NaOH溶液的试管中加入少量FeS04溶液,亚铁离子少全部转化为氢氧化亚铁,若该观点正确,应观察到的现象是无灰绿色出现,只有白色沉淀生成,
故答案为:析出白色沉淀;
②己知胶体粒子的吸附能力随温度升高而下降.向盛装FeSO4溶液的试管中滴加少量NaOH溶液,析出白色沉淀,沉淀迅速变为灰绿色,将此试管小心加热,吸附的亚铁离子离开沉淀,所以若观察到灰绿色沉淀变化为白色沉淀,说明上述解释成立,
故答案为:灰绿色沉淀变化为白色.
点评 本题考查了铁及其化合物性质的分析,主要是反应现象的解释和证明,注意题干信息的应用,题目较简单.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
17.下列说法正确的是( )
| A. | 增大反应物浓度,可增大活化分子百分数,从而使有效碰撞次数增多 | |
| B. | 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大 | |
| C. | 升高温度能使反应速率增大,主要原因是增加了反应物分子浓度 | |
| D. | 使用正催化剂能增大活化分子百分数,从而显著地增大化学反应速率 |
1.废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过下列方法回收钴、锂.
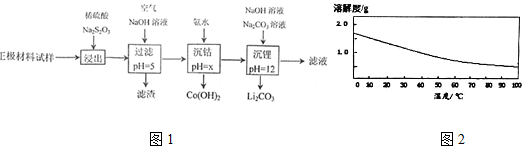
已知:
①Co(OH)2是两性氢氧化物.
②
请回答下列问题:
(1)浸出过程中为加快浸出速率,可以采取的措施有充分搅拌、升高温度(写出两点).
(2)浸出过程中Na2S2O3被氧化为Na2SO4的化学方程式为8LiCoO2+11H2SO4+Na2S2O3=4Li2SO4+8CoSO4+Na2SO4+11H2O.该过程中可用盐酸代替H2SO4和Na2S2O3,但缺点是生成氯气,污染环境.
(3)滤渣的成分为Al(OH)3、Fe(OH)3,充入空气的目的是将Fe2+被氧化为Fe3+.
(4)沉钴过程中不使用NaOH溶液的原因是Co(OH)2是两性氢氧化物,能与NaOH溶液反应导致沉淀的质量减少.当溶液中c(Co2+)≤10-5mol•L-1时即认为沉淀完全,则需要控制x≥9(Ksp[Co(OH)2]=1.0×10-15).制得的Co(OH)2不宜在空气中长期放置,会被空气中的O2氧化成Co(OH)3,化学反应方程式为4Co(OH)2+O2+2H2O=4Co(OH)3.
(5)碳酸锂的溶解度随温度的变化如右图所示,则洗涤碳酸锂沉淀时应选热水(填“热水”或“冷水”).

已知:
①Co(OH)2是两性氢氧化物.
②
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)3 |
| 开始沉淀的pH | 3.1 | 7.1 | 2.2 |
| 完全沉淀的pH | 4.7 | 9.7 | 3.7 |
(1)浸出过程中为加快浸出速率,可以采取的措施有充分搅拌、升高温度(写出两点).
(2)浸出过程中Na2S2O3被氧化为Na2SO4的化学方程式为8LiCoO2+11H2SO4+Na2S2O3=4Li2SO4+8CoSO4+Na2SO4+11H2O.该过程中可用盐酸代替H2SO4和Na2S2O3,但缺点是生成氯气,污染环境.
(3)滤渣的成分为Al(OH)3、Fe(OH)3,充入空气的目的是将Fe2+被氧化为Fe3+.
(4)沉钴过程中不使用NaOH溶液的原因是Co(OH)2是两性氢氧化物,能与NaOH溶液反应导致沉淀的质量减少.当溶液中c(Co2+)≤10-5mol•L-1时即认为沉淀完全,则需要控制x≥9(Ksp[Co(OH)2]=1.0×10-15).制得的Co(OH)2不宜在空气中长期放置,会被空气中的O2氧化成Co(OH)3,化学反应方程式为4Co(OH)2+O2+2H2O=4Co(OH)3.
(5)碳酸锂的溶解度随温度的变化如右图所示,则洗涤碳酸锂沉淀时应选热水(填“热水”或“冷水”).
11.阿司匹林的结构简式为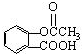 ,关于阿司匹林的叙述正确的是( )
,关于阿司匹林的叙述正确的是( )
 ,关于阿司匹林的叙述正确的是( )
,关于阿司匹林的叙述正确的是( )| A. | 阿司匹林属于抗生素 | |
| B. | 阿司匹林不能发生水解反应 | |
| C. | 阿司匹林具有解热镇痛作用 | |
| D. | 阿司匹林之所以成为经典药物是因为服用该药物没有不良反应 |
18.下列说法不正确的是( )
| A. | 磷酸的摩尔质量与阿伏加德罗常数(NA)个磷酸分子的质量在数值上相等 | |
| B. | 常温常压下,0.5NA个CO分子所占体积是11.2L | |
| C. | 1molNH4+中含有的电子数为10NA | |
| D. | 1L0.3mol/L的Na2SO4溶液中,含有Na+和 SO42-总数为0.9 NA |
15.实验室从海带灰中提取碘的操作过程中,仪器选用不正确的是( )
| A. | 称取5 g左右的干海带--托盘天平 | |
| B. | 过滤煮沸后的海带灰和水的混合物--漏斗 | |
| C. | 用蒸发结晶的方法从氧化后的海带灰浸取液中提取碘--蒸发皿 | |
| D. | 用四氯化碳从氧化后的海带灰浸取液中提取碘--长颈漏斗 |
16. 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成
甲醇:2H2(g)+CO(g)?CH3OH(g)
(1)下表所列数据是该反应在不同温度下的化学平衡常数(K)
①该反应的△H<0(填“>”、“<”或“=”).
②300℃时,将容器的容积压缩到原来的$\frac{1}{2}$,在其他条件不变的情况下,对平衡体系产生的影响是CD(填字母).
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加
D.重新平衡时$\frac{c({H}_{2})}{c(C{H}_{3}OH)}$减小
③某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则此时的温度为250℃,以CH3OH表示该过程的反应速率v(CH3OH)=0.08mol/(L.min).
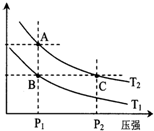
(2)如图表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A< C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A=C,由状态B到状态A,可采用升温的方法(填“升温”或“降温”).
 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)
(1)下表所列数据是该反应在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②300℃时,将容器的容积压缩到原来的$\frac{1}{2}$,在其他条件不变的情况下,对平衡体系产生的影响是CD(填字母).
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加
D.重新平衡时$\frac{c({H}_{2})}{c(C{H}_{3}OH)}$减小
③某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则此时的温度为250℃,以CH3OH表示该过程的反应速率v(CH3OH)=0.08mol/(L.min).
(2)如图表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A< C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A=C,由状态B到状态A,可采用升温的方法(填“升温”或“降温”).