题目内容
3.下列说法正确的是( )| A. | 滴有酚酞的NaOH溶液中通入SO2气体,溶液红色消失,证明SO2具有漂白性 | |
| B. | 配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会造成所配溶液浓度偏高 | |
| C. | 硅单质是制造光导纤维的材料 | |
| D. | 氯水放置数天后,pH会变大 |
分析 A.二氧化硫是碱性氧化物和碱反应生成盐和水,二氧化硫的漂白性是结合有色物质生成无色的不稳定的化合物;
B.根据c=$\frac{n}{V}$可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量n和溶液的体积V引起的,误差分析时,关键要看配制过程中引起n和V怎样的变化:若n比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若n比理论值大,或V比理论值小时,都会使所配溶液浓度偏大;
C.硅晶体是半导体做太阳能电池板、电脑芯片等,二氧化硅是光导纤维的成分;
D.氯水放置数天后,次氯酸分解生成盐酸,酸性增强,PH将变小.
解答 解:A.滴有酚酞的NaOH溶液中通入SO2气体,是二氧化硫和氢氧化钠反应生成亚硫酸钠和水,溶液中氢氧根离子浓度减小溶液红色消失,不是二氧化硫的漂白性,故A错误;
B.定容时俯视刻度线观察液面、溶液的体积偏小,配制溶液的浓度偏大,故B正确;
C.二氧化硅是制造光导纤维的材料,故C错误;
D.氯气与水发生:Cl2+H2O?HClO+HCl,其中HClO见光易分解而变质,久置后溶液PH变小,故D错误;
故选B.
点评 本题考查了物质性质、溶液配制,注意物质特征性质的理解应用,掌握基础是解题关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列关于钠的叙述错误的是( )
| A. | 实验后剩余少量钠可放回原试剂瓶中 | |
| B. | 用一般的化学还原法不能制取金属钠 | |
| C. | 某物质的焰色反应为黄色,则该物质一定含钠元素 | |
| D. | 钠可以用少量水密封保存 |
14.下列物质除杂(括号内物质为杂质)所用试剂正确的是( )
| 物 质 | 试 剂 | |
| A | Na2SO4溶液(NaBr) | Cl2 |
| B | FeCl2 溶液(FeCl3) | Cu |
| C | CO2(CO) | 通入O2燃烧 |
| D | CO2(HCl) | 饱和NaHCO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
11.某只含有C、H、O、N的有机物的简易球棍模型如图所示,下列关于该有机物的说法不正确的是( )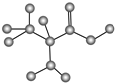

| A. | 该有机物属于氨基酸 | |
| B. | 该有机物的分子式为C3H7NO2 | |
| C. | 该有机物与CH3CH2CH2NO2互为同分异构体 | |
| D. | 一定条件下不能生成高分子化合物 |
15.下列实验操作:①取液体试剂,②萃取,③溶解,④过滤,⑤蒸发.一定要用玻璃棒的是( )
| A. | ①②③ | B. | ②③④ | C. | ①②⑤ | D. | ③④⑤ |
12.金属钠与下列物质的溶液反应,既有沉淀生成又有气体放出的是( )
| A. | Mg(NO3)2 | B. | HNO3 | C. | Na2SO4 | D. | NH4Cl |
13.实验室欲用Na2CO3•10H20晶体配制1mol/L的Na2CO3溶液100mL,下列说法正确的是( )
| A. | 要完成实验需称取10.6gNa2CO3•10H20晶体 | |
| B. | 本实验需用到的仪器只有药匙、玻璃棒、烧杯、胶头滴管和100 mL容量瓶 | |
| C. | 配制时若容量瓶不干燥,含有少量蒸馏水会导致浓度偏低 | |
| D. | 定容时用胶头滴管滴人的蒸馏水滴在容量瓶内部刻度线上方会导致浓度偏低 |
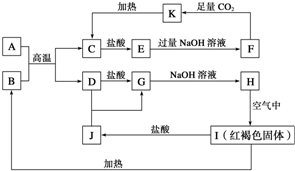 已知A~K均为中学化学的常见物质,它们之间的转化关系如下图所示,其中A是铝,且A+B→C+D是置换反应,反应过程中生成的水及其他部分产物已略去.
已知A~K均为中学化学的常见物质,它们之间的转化关系如下图所示,其中A是铝,且A+B→C+D是置换反应,反应过程中生成的水及其他部分产物已略去. .
.