题目内容
8.设阿伏加德罗常数的值为NA,下列说法中不正确的是( )| A. | 1mol甲基(-CH3)含有的电子数目为9NA | |
| B. | 28g乙烯和丙烯的混合气体中所含碳原子数为2NA | |
| C. | 1mol乙醛与足量新制Cu(OH)2悬浊液反应,转移电子数目为NA | |
| D. | 25℃时,1mol己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA |
分析 A、甲基不带电荷;
B、乙烯和丙烯的最简式均为CH2;
C、1mol乙醛能消耗2mol新制的氢氧化铜;
D、25℃时,1mol己烷完全燃烧后恢复至原状态,生成的气态物质只有二氧化碳.
解答 解:A、甲基不带电荷,故1mol甲基中含9NA个电子,故A正确;
B、乙烯和丙烯的最简式均为CH2,故28g乙烯和丙烯的混合物中含有的CH2的物质的量为2mol,则含2NA个碳原子,故B正确;
C、1mol乙醛能消耗2mol新制的氢氧化铜,将氢氧化铜中的+2价的铜还原为+1价,故转移2mol电子即2NA个,故C错误;
D、25℃时,1mol己烷完全燃烧后恢复至原状态,生成的气态物质只有二氧化碳,而1mol己烷完全燃烧能生成6mol二氧化碳,即6NA个气态分子,故D正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
18.某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,体积已换算成标准状态):
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大2~3min
(2)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)0.1mol/(L•min).
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液:
A.蒸馏水B.NaCl溶液C.Na2CO3 溶液D.CuSO4溶液你认为可行的是(填编号)AB.
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)0.1mol/(L•min).
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液:
A.蒸馏水B.NaCl溶液C.Na2CO3 溶液D.CuSO4溶液你认为可行的是(填编号)AB.
19.用价层电子对互斥理论预测H2S和PCl3的立体结构,两个结论都正确的是( )
| A. | 直线形;三角锥形 | B. | V形;三角锥形 | ||
| C. | 直线形;平面三角形 | D. | V形;平面三角形 |
16.有关化学键的说法正确的是( )
| A. | 全部由非金属元素构成的化合物一定是共价化合物 | |
| B. | 某元素的原子最外层只有一个电子,它跟卤素结合时,所形成的化学键一定是离子键 | |
| C. | 金属与非金属原子间只能形成离子键 | |
| D. | 含有共价键的化合物不一定是共价化合物 |
3.研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法不正确的是( )
| A. | 蒸馏常用于分离提纯液态有机混合物,温度计的水银球应位于支管口附近 | |
| B. | 核磁共振氢谱通常用于分析有机物的相对分子质量 | |
| C. | 燃烧法通常是研究和确定有机物成分的有效方法之一 | |
| D. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团 |
13.维生素C的结构简式为 ,丁香油酚的结构简式为:
,丁香油酚的结构简式为: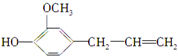 ,下列关于两者的说法正确的是( )
,下列关于两者的说法正确的是( )
 ,丁香油酚的结构简式为:
,丁香油酚的结构简式为: ,下列关于两者的说法正确的是( )
,下列关于两者的说法正确的是( )| A. | 均含酯基 | B. | 均含碳碳双键 | ||
| C. | 均含醇羟基和酚羟基 | D. | 均为芳香化合物 |
17.某工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).下列对该产品的描述不正确的是( )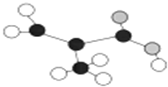

| A. | 官能团为碳碳双键、羧基 | B. | 与CH2=CHCOOCH3互为同分异构体 | ||
| C. | 能发生取代、加成和氧化反应 | D. | 分子中所有原子可能在同一平面 |
18.下列物质能与金属钠作用放出气体的是( )
| A. | C2H5OH | B. | CH4 | C. | C2H4 | D. | CH3COOCH2CH3 |
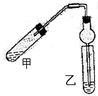 如图(铁架台、铁夹等省略)在试管甲中先加入碎瓷片,再加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上.在试管乙中加入5mL饱和碳酸钠溶液.按如图连接装置,用酒精灯对试管甲加热,当观察到试管乙中有明显现象时停止实验
如图(铁架台、铁夹等省略)在试管甲中先加入碎瓷片,再加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上.在试管乙中加入5mL饱和碳酸钠溶液.按如图连接装置,用酒精灯对试管甲加热,当观察到试管乙中有明显现象时停止实验