题目内容
有机化合物F是合成电子薄膜材料高聚物Z 和增塑剂P的重要原料.
(1)某同学设计了由乙烯合成高聚物Z的3条路线(I、II、III)如图所示.
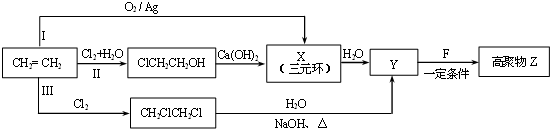
①3条合成路线中,你认为符合“原子经济”要求的合成路线是(填序号“I”、“II”或“III”) .
②X的结构简式是 .
③1mol F在O2中充分燃烧,消耗7.5mol O2,生成8molCO2 和3molH2O,1mol F与足量NaHCO3溶液反应生成2mol CO2.其分子内的氢原子处于3种不同的化学环境.
F分子中含有的含氧官能团的名称是 .
Y+F→Z反应的化学方程式是 .
(2)已知: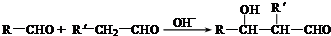 (R、R'代表烃基或氢原子).合成P的路线如图所示.D分子中有8个碳原子,其主链上有6个碳原子,且分子内只含有两个-CH3.
(R、R'代表烃基或氢原子).合成P的路线如图所示.D分子中有8个碳原子,其主链上有6个碳原子,且分子内只含有两个-CH3.
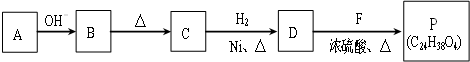
①A→B反应的化学方程式是 .
②B→C的反应中,B分子在加热条件下脱去一个水分子,生成C;C分子中只有1个碳原子上无氢原子.C的结构简式是 .
③P的结构简式是 .
④符合下列条件的B的同分异构体共有(填数字) 种.
a.在酸性条件下水解为M和N b.一定条件下M可以转化为N.
(1)某同学设计了由乙烯合成高聚物Z的3条路线(I、II、III)如图所示.

①3条合成路线中,你认为符合“原子经济”要求的合成路线是(填序号“I”、“II”或“III”)
②X的结构简式是
③1mol F在O2中充分燃烧,消耗7.5mol O2,生成8molCO2 和3molH2O,1mol F与足量NaHCO3溶液反应生成2mol CO2.其分子内的氢原子处于3种不同的化学环境.
F分子中含有的含氧官能团的名称是
Y+F→Z反应的化学方程式是
(2)已知:
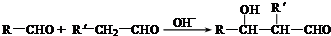 (R、R'代表烃基或氢原子).合成P的路线如图所示.D分子中有8个碳原子,其主链上有6个碳原子,且分子内只含有两个-CH3.
(R、R'代表烃基或氢原子).合成P的路线如图所示.D分子中有8个碳原子,其主链上有6个碳原子,且分子内只含有两个-CH3.
①A→B反应的化学方程式是
②B→C的反应中,B分子在加热条件下脱去一个水分子,生成C;C分子中只有1个碳原子上无氢原子.C的结构简式是
③P的结构简式是
④符合下列条件的B的同分异构体共有(填数字)
a.在酸性条件下水解为M和N b.一定条件下M可以转化为N.
考点:有机物的推断
专题:有机物的化学性质及推断
分析:(1)乙烯在Ag作催化剂条件下被氧气氧化生成X,X是三元环,且ClCH2CH2OH和氢氧化钙反应也生成X,则X为环氧乙烷,其结构简式为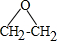 ,1,2-二氯乙烷和氢氧化钠的水溶液加热生成Y,则Y的结构简式为HOCH2CH2OH,1mol F在O2中充分燃烧,消耗7.5mol O2,生成8molCO2 和3molH2O,根据原子守恒知一个F分子中含有8个C原子、6个H原子、4个O原子,1mol F与足量NaHCO3溶液反应生成2mol CO2,说明F中含有2个羧基,其分子内的氢原子处于3种不同的化学环境,则F的结构简式为
,1,2-二氯乙烷和氢氧化钠的水溶液加热生成Y,则Y的结构简式为HOCH2CH2OH,1mol F在O2中充分燃烧,消耗7.5mol O2,生成8molCO2 和3molH2O,根据原子守恒知一个F分子中含有8个C原子、6个H原子、4个O原子,1mol F与足量NaHCO3溶液反应生成2mol CO2,说明F中含有2个羧基,其分子内的氢原子处于3种不同的化学环境,则F的结构简式为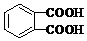 ,Y和F在浓硫酸作催化剂、加热条件下发生缩聚反应生成Z,则Z的结构简式为
,Y和F在浓硫酸作催化剂、加热条件下发生缩聚反应生成Z,则Z的结构简式为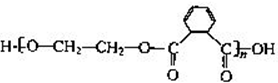 ;
;
(2)D分子中有8个碳原子,其主链上有6个碳原子,且分子内只含有两个-CH3,可知A为CH3CH2CH2CHO,B为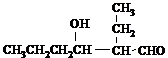 ,C为
,C为 ,D为
,D为 ,P为
,P为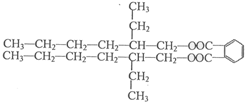 ,据此分析解答.
,据此分析解答.
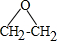 ,1,2-二氯乙烷和氢氧化钠的水溶液加热生成Y,则Y的结构简式为HOCH2CH2OH,1mol F在O2中充分燃烧,消耗7.5mol O2,生成8molCO2 和3molH2O,根据原子守恒知一个F分子中含有8个C原子、6个H原子、4个O原子,1mol F与足量NaHCO3溶液反应生成2mol CO2,说明F中含有2个羧基,其分子内的氢原子处于3种不同的化学环境,则F的结构简式为
,1,2-二氯乙烷和氢氧化钠的水溶液加热生成Y,则Y的结构简式为HOCH2CH2OH,1mol F在O2中充分燃烧,消耗7.5mol O2,生成8molCO2 和3molH2O,根据原子守恒知一个F分子中含有8个C原子、6个H原子、4个O原子,1mol F与足量NaHCO3溶液反应生成2mol CO2,说明F中含有2个羧基,其分子内的氢原子处于3种不同的化学环境,则F的结构简式为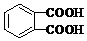 ,Y和F在浓硫酸作催化剂、加热条件下发生缩聚反应生成Z,则Z的结构简式为
,Y和F在浓硫酸作催化剂、加热条件下发生缩聚反应生成Z,则Z的结构简式为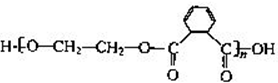 ;
;(2)D分子中有8个碳原子,其主链上有6个碳原子,且分子内只含有两个-CH3,可知A为CH3CH2CH2CHO,B为
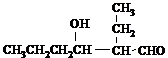 ,C为
,C为 ,D为
,D为 ,P为
,P为 ,据此分析解答.
,据此分析解答.解答:
解:(1)乙烯在Ag作催化剂条件下被氧气氧化生成X,X是三元环,且ClCH2CH2OH和氢氧化钙反应也生成X,则X为环氧乙烷,其结构简式为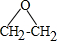 ,1,2-二氯乙烷和氢氧化钠的水溶液加热生成Y,则Y的结构简式为HOCH2CH2OH,1mol F在O2中充分燃烧,消耗7.5mol O2,生成8molCO2 和3molH2O,根据原子守恒知一个F分子中含有8个C原子、6个H原子、4个O原子,
,1,2-二氯乙烷和氢氧化钠的水溶液加热生成Y,则Y的结构简式为HOCH2CH2OH,1mol F在O2中充分燃烧,消耗7.5mol O2,生成8molCO2 和3molH2O,根据原子守恒知一个F分子中含有8个C原子、6个H原子、4个O原子,
1mol F与足量NaHCO3溶液反应生成2mol CO2,说明F中含有2个羧基,其分子内的氢原子处于3种不同的化学环境,则F的结构简式为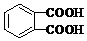 ,Y和F在浓硫酸作催化剂、加热条件下发生缩聚反应生成Z,则Z的结构简式为
,Y和F在浓硫酸作催化剂、加热条件下发生缩聚反应生成Z,则Z的结构简式为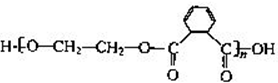 ;
;
①由乙烯合成高聚物Z的3条路线Ⅰ无副产物,符合“原子经济”要求,Ⅱ、Ⅲ都有副产物CaCl2和水,不符合“原子经济”要求,
故答案为:I;
②通过以上分析知,X的结构简式是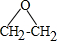 ,故答案为:
,故答案为: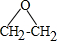 ;
;
③通过以上分析知,F的结构简式为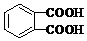 ,其官能团名称是羧基;
,其官能团名称是羧基;
Y和F在浓硫酸作催化剂、加热条件下发生缩聚反应生成Z,该反应方程式为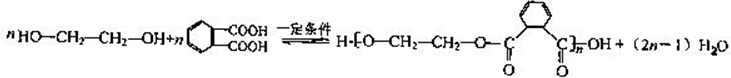 ,
,
故答案为:羧基;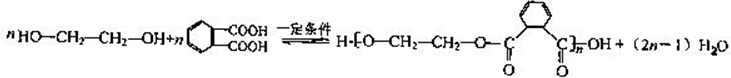 .
.
(2)D分子中有8个碳原子,其主链上有6个碳原子,且分子内只含有两个-CH3,可知A为CH3CH2CH2CHO,B为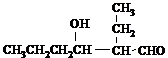 ,C为
,C为 ,D为
,D为 ,P为
,P为 ,
,
①A为CH3CH2CH2CHO,B为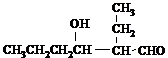 ,可在碱性条件下发生水解反应生成,反应的方程式为
,可在碱性条件下发生水解反应生成,反应的方程式为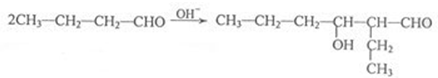 ,
,
故答案为: ;
;
②通过以上分析知,C的结构简式 ,故答案为:
,故答案为: ;
;
③通过以上分析知P的结构简式是 ,故答案为:
,故答案为: ;
;
④符合条件的B的同分异构体有CH3-CH2-CH2COO-CH2-CH2-CH2-CH3和CH3CH(CH3)COOCH2CH(CH3)CH3,共2种,故答案为:2.
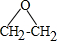 ,1,2-二氯乙烷和氢氧化钠的水溶液加热生成Y,则Y的结构简式为HOCH2CH2OH,1mol F在O2中充分燃烧,消耗7.5mol O2,生成8molCO2 和3molH2O,根据原子守恒知一个F分子中含有8个C原子、6个H原子、4个O原子,
,1,2-二氯乙烷和氢氧化钠的水溶液加热生成Y,则Y的结构简式为HOCH2CH2OH,1mol F在O2中充分燃烧,消耗7.5mol O2,生成8molCO2 和3molH2O,根据原子守恒知一个F分子中含有8个C原子、6个H原子、4个O原子,1mol F与足量NaHCO3溶液反应生成2mol CO2,说明F中含有2个羧基,其分子内的氢原子处于3种不同的化学环境,则F的结构简式为
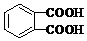 ,Y和F在浓硫酸作催化剂、加热条件下发生缩聚反应生成Z,则Z的结构简式为
,Y和F在浓硫酸作催化剂、加热条件下发生缩聚反应生成Z,则Z的结构简式为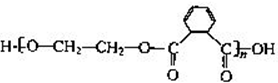 ;
;①由乙烯合成高聚物Z的3条路线Ⅰ无副产物,符合“原子经济”要求,Ⅱ、Ⅲ都有副产物CaCl2和水,不符合“原子经济”要求,
故答案为:I;
②通过以上分析知,X的结构简式是
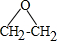 ,故答案为:
,故答案为: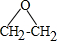 ;
;③通过以上分析知,F的结构简式为
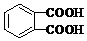 ,其官能团名称是羧基;
,其官能团名称是羧基;Y和F在浓硫酸作催化剂、加热条件下发生缩聚反应生成Z,该反应方程式为
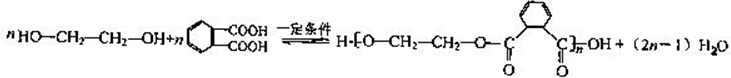 ,
,故答案为:羧基;
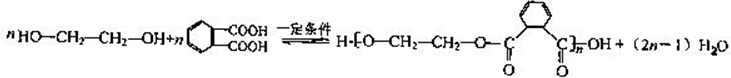 .
.(2)D分子中有8个碳原子,其主链上有6个碳原子,且分子内只含有两个-CH3,可知A为CH3CH2CH2CHO,B为
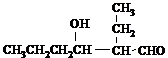 ,C为
,C为 ,D为
,D为 ,P为
,P为 ,
,①A为CH3CH2CH2CHO,B为
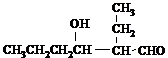 ,可在碱性条件下发生水解反应生成,反应的方程式为
,可在碱性条件下发生水解反应生成,反应的方程式为 ,
,故答案为:
 ;
;②通过以上分析知,C的结构简式
 ,故答案为:
,故答案为: ;
;③通过以上分析知P的结构简式是
 ,故答案为:
,故答案为: ;
;④符合条件的B的同分异构体有CH3-CH2-CH2COO-CH2-CH2-CH2-CH3和CH3CH(CH3)COOCH2CH(CH3)CH3,共2种,故答案为:2.
点评:本题考查有机物推断,侧重考查分析、推断、知识迁移能力,熟练掌握常见有机物的官能团及其性质,注意结合题给信息进行推断,题目难度中等.

练习册系列答案
相关题目
0.1mol/L氨水中,溶液中随着水量的增加而减少的是( )
A、
| ||
B、
| ||
| C、C(H+)和C(OH-)的乘积 | ||
| D、OH-的物质的量 |
将下列物质分别投入到FeCl3溶液中,没有气体产生,但有沉淀生成的是( )
| A、Na |
| B、Na2O2 |
| C、Na2O |
| D、NaCl |
PCl3和PCl5都是重要的化工原料.将PCl3(g) 和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生下述反应,并于10 min时达到平衡:PCl3(g)+Cl3(g)?PCl3(g).有关数据如下:
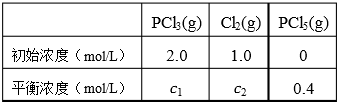
下列判断不正确的是( )

下列判断不正确的是( )
| A、10 min内,v(Cl2)=0.04 mol/(L?min) |
| B、当容器中Cl2为1.2 mol时,反应达到平衡 |
| C、升高温度(T1<T2),反应的平衡常数减小,平衡时PCl3的转化率变大 |
| D、平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L |
下列能达到实验目的是( )
A、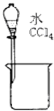 分离水和CCl4 |
B、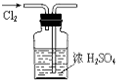 干燥Cl2 |
C、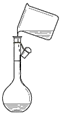 转移溶液 |
D、 蒸发食盐水 |
为达到下列实验目的,所采用的方法正确的是( )
| A、从溴水中提取溴--分液 |
| B、分离水和汽油的混合物--蒸馏 |
| C、从硝酸钾和氯化钾混合液中获取硝酸钾--蒸发 |
| D、分离饱和食盐水和沙子的混合物--过滤 |
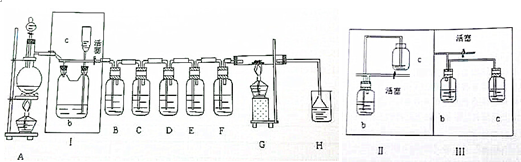
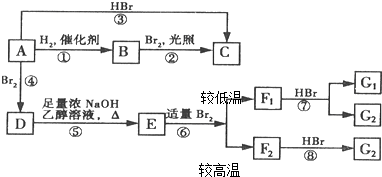
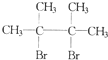 F1和F2为同分异构体,G1和G2互为同分异构体)
F1和F2为同分异构体,G1和G2互为同分异构体)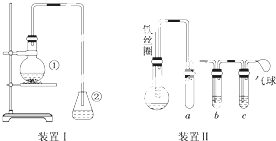 为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验:
为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验: