题目内容
8.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)═CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应为吸热反应(填“吸热”、“放热”),写出该反应的平衡常数表达式:K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$
(2)能使该反应的反应速率增大,且平衡向正反应方向移动的是bc.
a.及时分离出CO气体 b.适当升高温度
c.增大CO2的浓度 d.选择高效催化剂
(3)能判断该反应是否达到化学平衡状态的依据是bc.
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(5)若在(4)所处的温度下,在1L的密闭容器中,加入2molCO2和3molH2充分反应达平衡时,H2的物质的量为b,CO2的物质的量为c.
a.等于1.0mol b.大于1.0mol c.大于0.5mol,小于1.0mol d.无法确定.
分析 (1)依据图表数据分析,平衡常数随温度升高增大,说明温度升高平衡正向进行,正反应是吸热反应;平衡常数是利用生成物平衡浓度的幂次方乘积除以反应物平衡浓度幂次方乘积得到;
(2)a.及时分离出CO气体,反应速率减小,平衡正向移动;
b.适当升高温度,反应速率加快,平衡正向移动;
c.增大CO2的浓度反应速率加快,平衡正向移动;
d.选择高效催化剂,能使该反应的反应速率增大,但平衡不移动;
(3)化学平衡状态的标志:正逆反应速率相等;
(4)某温度下,各物质的平衡浓度符合下式:c(CO2).c(H2)=c(CO).c(H2O),说明 K=1,由此分析解答;
(5)依据化学平衡三段式列式和平衡常数概念计算消耗氢气物质的量计算得到平衡状态下的物质的量.
解答 解:(1)图表数据分析,平衡常数随温度升高增大,说明温度升高平衡正向进行,正反应是吸热反应;CO2(g)+H2(g)═CO(g)+H2O(g),平衡常数是利用生成物平衡浓度的幂次方乘积除以反应物平衡浓度幂次方乘积得到,K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$,
故答案为:吸热;$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$;
(2)a.及时分离出CO气体,反应速率减小,平衡正向移动,故错误;
b.适当升高温度,反应速率加快,平衡正向移动,故正确;
c.增大CO2的浓度反应速率加快,平衡正向移动,故正确;
d.选择高效催化剂,能使该反应的反应速率增大,但平衡不移动,故错误;故选bc;
(3)a、反应是一个反应前后体积不变的反应,压强的改变不会要引起平衡移动,故a错误;
b、化学平衡时,各组分的浓度不随时间的改变而改变,故b正确;
c、化学平衡状态的标志是v正=v逆,所以v正(H2)=v逆(H2O)表明反应达到平衡状态,故c正确;
d、c(CO2)=c(CO)时,不能表明正逆反应速率相等,不一定达到了平衡状态,故d错误.
故选bc;
(4)某温度下,各物质的平衡浓度符合下式:c(CO2).c(H2)=c(CO).c(H2O),说明 K=1,对应的温度是830℃,故答案为:830℃.
(5)若在(3)所处的温度下,在1L的密闭容器中,加入2mol CO2和3mol H2充分反应达平衡时,设氢气消耗物质的量为x;
CO2(g)+H2(g)?CO(g)+H2O(g)
起始量(mol/L) 2 3 0 0
变化量(mol/L) x x x x
平衡量(mol/L) 2-x 3-x x x
K=$\frac{{x}^{2}}{(2-x)•(3-x)}$=1,计算得到:x=1.2,反应达平衡时,H2的物质的量3mol-1.2mol=1.8mol;CO2的物质的量为0.8mol,
故答案为:b;c.
点评 本题考查学生对平衡常数K的改变与平衡移动之间的关系的理解,以及影响化学平衡的因素,及利用平衡常数K进行简单的计算能力,难度不大.

| A. | 1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L | |
| B. | 从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液中氢离子的浓度为2 mol/L | |
| C. | 配制480 mL 0.5 mol/L的CuSO4溶液,需称取62.5 g胆矾 | |
| D. | 中和100 mL 1mol/L的H2SO4溶液,需NaOH为4 g |
| A. | 溶液 | B. | 悬浊液 | C. | 乳浊液 | D. | 胶体 |
| A. | Mg2+、Na+、SO42-、Cl- | B. | Na+、Cu2+、SO42-、NO3- | ||
| C. | Na+、K+、OH-、Cl- | D. | Ba2+、CO32-、NO3-、K+ |
 下图曲线a表示反应X(g)+Y(g)+N(s)?Z(g)+M(g)△H<0进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
下图曲线a表示反应X(g)+Y(g)+N(s)?Z(g)+M(g)△H<0进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )| A. | 升高温度 | B. | 加大N的投入量 | C. | 添加催化剂 | D. | 加大X的投入量 |
 在一定条件下,反应X(g)+3Y(g)?2Z(g)△H=-92.4 kJ/mol,X的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
在一定条件下,反应X(g)+3Y(g)?2Z(g)△H=-92.4 kJ/mol,X的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )| A. | 图中A、B两点,达到相同的平衡体系 | |
| B. | 上述反应在达到平衡后,增大压强,H2的转化率提高 | |
| C. | 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小 | |
| D. | 将1.0 mol X、3.0 mol Y,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ |

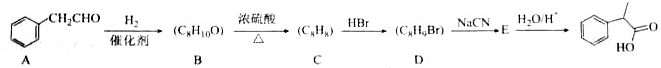
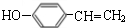 .
.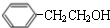 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$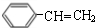 +H2O;C→D的反应类型为加成反应
+H2O;C→D的反应类型为加成反应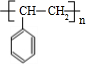 .
. 某位同学在查阅资料时发现含氮化合物有以下性质:
某位同学在查阅资料时发现含氮化合物有以下性质: