题目内容
已知H2(g)+Cl2(g)=2HCl(g);ΔH=-184.6kJ/mo1,则反应HCl(g)= H2(g)+
H2(g)+ Cl2(g)的ΔH为
Cl2(g)的ΔH为
[ ]
A.+184.6kJ/mol
B.-92.3kJ/mol
C.-369.2kJ/mol
D.+92.3kJ/mol
答案:D
解析:
解析:
|
导解:2HCl(g)=H2(g)+Cl2(g)是原反应的逆反应,所以反应热的符号相反,数值相等,ΔH=+184.6kJ/mol.而HCl(g)= |

练习册系列答案
相关题目
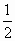 H2(g)+
H2(g)+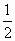 Cl2(g)的系数是2HCl(g)
Cl2(g)的系数是2HCl(g) H2(g)+Cl2(g)的一半,所以反应热也为它的一半,ΔH=+92.3kJ/mol.
H2(g)+Cl2(g)的一半,所以反应热也为它的一半,ΔH=+92.3kJ/mol. CH4 是一种清洁、高效、具有优良的环保性能的燃料,其燃烧热为890.3KJ?mol-1.它可以作为燃料电池的燃料.
CH4 是一种清洁、高效、具有优良的环保性能的燃料,其燃烧热为890.3KJ?mol-1.它可以作为燃料电池的燃料.


