题目内容
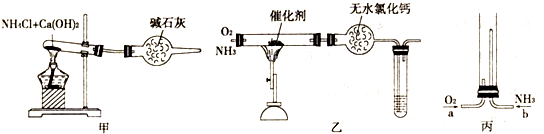
资料:“氨气可在纯氧中安静燃烧…”.某校化学小组学生设计如图装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验.

(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式是
②将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:(a)两气体中,先通入的气体是
分析:(1)碳酸铵受热分解生成氨气、二氧化碳、水蒸气,通过盛有碱石灰的干燥管除去二氧化碳和水蒸气得到干燥纯净的氨气;
(2)①NH3与过量O2在催化剂、加热条件下发生反应:4NH3+5O2
4NO+6H2O,生成的NO在试管内被过量的O2氧化为红棕色的NO2气体,未反应的氨气和生成的水用装有无水氯化钙的干燥管吸收;生成的氨气与氧气反应生成红棕色的二氧化氮气体,二氧化氮和水反应生成硝酸,溶液显酸性使湿润变红色;
②若先通入NH3,NH3在空气中不能燃烧,容易逸出污染空气,但是氨气在纯氧中能充分燃烧,生成物为无污染的氮气和水.
(2)①NH3与过量O2在催化剂、加热条件下发生反应:4NH3+5O2
| ||
| 高温高压 |
②若先通入NH3,NH3在空气中不能燃烧,容易逸出污染空气,但是氨气在纯氧中能充分燃烧,生成物为无污染的氮气和水.
解答:解:(1)碳酸铵受热分解方程式:(NH4)2CO3
2NH3+H2O+CO2,通过盛有碱石灰的干燥管除去二氧化碳和水蒸气得到干燥纯净的氨气;
故答案为:(NH4)2CO3
2NH3+H2O+CO2;除去二氧化碳和水蒸气;
(2)①NH3与过量O2在催化剂、加热条件下发生反应:4NH3+5O2
4NO+6H2O;用盛有无水氯化钙的干燥管吸收未反应的氨气和生成的水;2NO+O2=2NO2二氧化氮是红棕色的气体;二氧化氮溶于水与水发生反应:3NO2+2H2O=2HNO3+NO,硝酸具有酸性使石蕊试液变红;
故答案为:4NH3+5O2
4NO+6H2O;吸收未反应的氨气和生成的水;红棕色;2NO+O2=2NO2;红;3NO2+2H2O=2HNO3+NO;
②若先通入NH3,NH3在空气中不能点燃,容易逸出污染空气,但是氨气在纯氧中能充分燃烧,生成物为无污染的氮气和水,反应方程式为:4NH3+3O2
2N2+6H2O;
故答案为:a)先通入氧气,NH3在空气中不能燃烧,容易逸出污染空气,但是氨气在纯氧中能充分燃烧;
b)4NH3+3O2
2N2+6H2O.
| ||
故答案为:(NH4)2CO3
| ||
(2)①NH3与过量O2在催化剂、加热条件下发生反应:4NH3+5O2
| ||
| 高温高压 |
故答案为:4NH3+5O2
| ||
| 高温高压 |
②若先通入NH3,NH3在空气中不能点燃,容易逸出污染空气,但是氨气在纯氧中能充分燃烧,生成物为无污染的氮气和水,反应方程式为:4NH3+3O2
| ||
故答案为:a)先通入氧气,NH3在空气中不能燃烧,容易逸出污染空气,但是氨气在纯氧中能充分燃烧;
b)4NH3+3O2
| ||
点评:本题考查了氨气的制法和性质,题目难度不大,侧重考查学生分析实验,解决问题的能力.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目