题目内容
有关下列溶液的叙述不正确的是( )
| A、C H3COOH与CH3COONa的混合溶液中:c(CH3COO-)+c(OH-)=c(Na+)+c(H+) |
| B、常温下,0.1mol.L-1CH3COONa溶液和0.1mol.L-1NaHCO3溶液,NaHCO3溶液的pH大 |
| C、0.1mol.L-1的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| D、将l mol KC1、l mol KHS溶于水配成的混合溶液中:n(K+)=n(S2-)+n(HS-)+n(H2S) |
考点:离子浓度大小的比较
专题:
分析:A、根据电荷守恒,得c(CH3COO-)+c(OH-)=c(Na+)+c(H+);
B、对应酸越弱,阴离子水解程度越大,溶液碱性越强,酸性强弱为:CH3COOH>H2CO3,pH由大到小的排列顺序:NaHCO3>CH3COONa;
C、(NH4)2SO4是强酸弱碱盐,且二元的铵根离子浓度最大,所以离子浓度大小为:c(NH4+)>c(SO42-)>c(H+)>c(OH-);
D、根据钾和硫的物质的量之比为2:1,而硫元素在溶液中存在形式有三种,得到n(K+)=2[n(S2-)+n(HS-)+n(H2S)].
B、对应酸越弱,阴离子水解程度越大,溶液碱性越强,酸性强弱为:CH3COOH>H2CO3,pH由大到小的排列顺序:NaHCO3>CH3COONa;
C、(NH4)2SO4是强酸弱碱盐,且二元的铵根离子浓度最大,所以离子浓度大小为:c(NH4+)>c(SO42-)>c(H+)>c(OH-);
D、根据钾和硫的物质的量之比为2:1,而硫元素在溶液中存在形式有三种,得到n(K+)=2[n(S2-)+n(HS-)+n(H2S)].
解答:
解:A、根据电荷守恒,得c(CH3COO-)+c(OH-)=c(Na+)+c(H+),故A正确;
B、对应酸越弱,阴离子水解程度越大,溶液碱性越强,酸性强弱为:CH3COOH>H2CO3,pH由大到小的排列顺序:NaHCO3>CH3COONa,所以,NaHCO3溶液的pH大,故B正确;
C、(NH4)2SO4是强酸弱碱盐,且二元的铵根离子浓度最大,所以离子浓度大小为:c(NH4+)>c(SO42-)>c(H+)>c(OH-),故C错误;
D、根据钾和硫的物质的量之比为2:1,而硫元素在溶液中存在形式有三种,得到n(K+)=2[n(S2-)+n(HS-)+n(H2S)],故D错误;
故选CD.
B、对应酸越弱,阴离子水解程度越大,溶液碱性越强,酸性强弱为:CH3COOH>H2CO3,pH由大到小的排列顺序:NaHCO3>CH3COONa,所以,NaHCO3溶液的pH大,故B正确;
C、(NH4)2SO4是强酸弱碱盐,且二元的铵根离子浓度最大,所以离子浓度大小为:c(NH4+)>c(SO42-)>c(H+)>c(OH-),故C错误;
D、根据钾和硫的物质的量之比为2:1,而硫元素在溶液中存在形式有三种,得到n(K+)=2[n(S2-)+n(HS-)+n(H2S)],故D错误;
故选CD.
点评:本题考查了溶液pH的大小比较、电荷守恒和物料守恒的相关知识,题目难度不大,注意考虑电解质的强弱以及盐类的水解情况,试题侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
根据下列反应判断氧化剂的氧化性由强到弱的顺序正确的是( )
①Cl2+2KI══I2+2KCl
②2FeCl3+2HI══I2+2FeCl2+2HCl
③2FeCl2+Cl2══2FeCl3
④I2+SO2+2H2O══2HI+H2SO4.
①Cl2+2KI══I2+2KCl
②2FeCl3+2HI══I2+2FeCl2+2HCl
③2FeCl2+Cl2══2FeCl3
④I2+SO2+2H2O══2HI+H2SO4.
| A、Cl2>I2>Fe3+>SO2 |
| B、Cl2>Fe3++>I2>SO2 |
| C、Fe3+>Cl2>I2>SO2 |
| D、Cl2>Fe3+>SO2>I2 |
下列说法不正确的是( )
| A、硬铝、碳素钢都是合金材料;合成纤维、光导纤维都是有机高分子化合物 |
| B、油脂在碱的作用下可发生水解,工业上利用该反应生产肥皂 |
| C、处理废水时可加入明矾作为混凝剂,以吸附水中的杂质 |
| D、推广可利用太阳能、风能的城市照明系统,发展低碳经济和循环经济,有利于改善环境质量 |
一定条件下,卤代烃和金属钠能发生伍兹反应:RX+2Na+RX→R-R+2NaX,反应中有C-X键的断裂和C-C键的形成.据此,以下卤代烃伍兹反应的可能产物(不考虑NaX)及命名合理的是( )
| A、一氯甲烷和2-氯丙烷:正丁烷 |
| B、2,2-二甲基-1-氯丙烷与一氯甲烷:3,3-二甲基丁烷 |
| C、1,5-二氯戊烷:环戊烷 |
| D、四氯化碳:金刚石 |
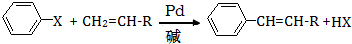 (X为卤原子,R为取代基)
(X为卤原子,R为取代基)