题目内容
5.选择下列实验方法分离物质,将分离方法的序号填在横线上.A.萃取分液 B.升华 C.结晶 D.过滤 E.蒸馏 F.分液
(1)分离饱和食盐水与沙子的混合物D
(2)从碘水中提取碘单质A
(3)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物E.
分析 (1)沙子不溶于水;
(2)碘易溶于有机溶剂;
(3)二者沸点不同,可蒸馏分离.
解答 解:(1)沙子不溶于水,可用过滤的方法分离,故答案为:D;
(2)沙子不溶于水,可用萃取的方法分离,故答案为:A;
(3)二者沸点不同,可蒸馏分离,故答案为:E.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
15.下列反应进行分类时,既属于氧化还原反应又属于置换反应的是( )
| A. | 4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$Fe+4CO2 | B. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O |
13.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,S2和S8的固体混合物共6.4g,其中所含硫原子数一定为0.2NA | |
| B. | 将1molFeCl3滴入足量沸水中,所分散系中粒子数目小于NA | |
| C. | 6.4g铜与硫反应时,铜失去的电子数为0.2NA | |
| D. | 标准状况下,44.8L NO与22.4L O2混合后气体中分子总数为2NA |
20.设NA为阿伏加德罗常数,以下说法正确的是( )
| A. | 标准状况下,22.4 L乙醇中分子数为NA | |
| B. | 含有NA个氦原子的氦气在标准状况下的体积约为22.4L | |
| C. | 1.8g的NH4+中含有的电子数为1.1NA | |
| D. | 在1 L 2 mol/L的盐酸中,存在2NA个氯化氢分子 |
17.下列实验原理,操作或装置(略去部分夹持仪器)正确的是( )
| A. |  配制溶液 | B. |  中和滴定 | ||
| C. |  除去溴苯中少量的溴单质 | D. |  制取并收集氨气 |
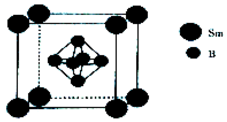 硼及其化合物在工农业生产中应用广泛.
硼及其化合物在工农业生产中应用广泛.
 用ClO2处理后的自来水中,ClO2的浓度应在0.10~0.80mg/L之间.用碘量法检测水中C1O2浓度的实验步骤如下:
用ClO2处理后的自来水中,ClO2的浓度应在0.10~0.80mg/L之间.用碘量法检测水中C1O2浓度的实验步骤如下: