题目内容
下列离子方程式正确的是:
| A、氢氧化铁中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| B、铝粉溶于氢氧化钠溶液中:Al+2OH-=AlO2-+H2↑ |
| C、在酸性的硫酸亚铁溶液中加入双氧水:2Fe2++H2O2+2H+=2Fe3++2H2O |
| D、硫化氢气体通入氯化铁溶液中:Fe3++H2S=Fe2++S↓+2H+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.三价铁离子具有氧化性,能够氧化碘离子;
B.电荷不守恒;
C.双氧水具有氧化性,能够氧化二价铁离子;
D.电荷不守恒.
B.电荷不守恒;
C.双氧水具有氧化性,能够氧化二价铁离子;
D.电荷不守恒.
解答:
解:A.氢氧化铁中加入氢碘酸,离子方程式:2Fe(OH)3+2I-+6H+=2Fe2++I2+6H2O,故A错误;
B.铝粉溶于氢氧化钠溶液中,离子方程式:2H2O+2Al+2OH-=2AlO2-+3H2↑,故B错误;
C.在酸性的硫酸亚铁溶液中加入双氧水,离子方程式:2Fe2++H2O2+2H+=2Fe3++2H2O,故C正确;
D.硫化氢气体通入氯化铁溶液中,离子方程式:2Fe3++H2S=2Fe2++S↓+2H+,故D错误;
故选:C.
B.铝粉溶于氢氧化钠溶液中,离子方程式:2H2O+2Al+2OH-=2AlO2-+3H2↑,故B错误;
C.在酸性的硫酸亚铁溶液中加入双氧水,离子方程式:2Fe2++H2O2+2H+=2Fe3++2H2O,故C正确;
D.硫化氢气体通入氯化铁溶液中,离子方程式:2Fe3++H2S=2Fe2++S↓+2H+,故D错误;
故选:C.
点评:本题考查了离子方程式的书写,明确反应的实质是解题关键,注意离子方程式应遵循电荷守恒,原子个数守恒,题目难度不大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
下列离子方程式书写正确的是( )
| A、氢氧化铁溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O |
| B、氯气溶于水:Cl2+H2O=2H++ClO-+Cl- |
| C、溴化亚铁溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
| D、向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
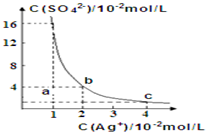 某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:下列有关Ag2SO4说法正确的是( )
某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:下列有关Ag2SO4说法正确的是( )| A、含有大量SO42-的溶液中肯定不存在Ag+ |
| B、Ag2SO4的溶度积常数(Ksp)为8×10-4 |
| C、a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点 |
| D、0.02mol?L-1的AgNO3溶液与0.2mol?L-1的Na2SO4溶液等体积混合不会生成沉淀 |
