题目内容
(1)图1为阳离子交换膜法电解饱和食盐水(滴有酚酞)原理示意图,E口产生H2,电解食盐水的离子方程式为: ,溶液变红色的是: 区(填A或B).
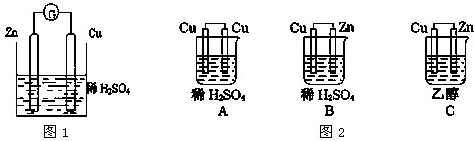
(2)电化腐蚀是钢铁发生腐蚀的主要原因,又可分为吸氧腐蚀和析氢腐蚀,发生吸氧腐蚀的电极反应式:负极 、正极 .
(3)图2是一套电化学实验装置,图2中C、D均为铂电极,U为盐桥,G是灵敏电流计
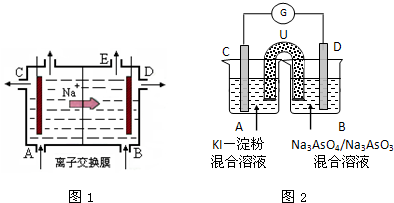
此装置中进行的反应是可逆反应,其反应方程式式为:AsO43-+2I-+H+?AsO33-+I2+H2O,向B杯中加入适量较浓的硫酸,发现G的指针向右偏移.此时A杯中的主要实验现象是 ,D电极上的电极反应式为 .
(2)电化腐蚀是钢铁发生腐蚀的主要原因,又可分为吸氧腐蚀和析氢腐蚀,发生吸氧腐蚀的电极反应式:负极
(3)图2是一套电化学实验装置,图2中C、D均为铂电极,U为盐桥,G是灵敏电流计

此装置中进行的反应是可逆反应,其反应方程式式为:AsO43-+2I-+H+?AsO33-+I2+H2O,向B杯中加入适量较浓的硫酸,发现G的指针向右偏移.此时A杯中的主要实验现象是
考点:电解原理,金属的电化学腐蚀与防护
专题:电化学专题
分析:(1)根据产物和阳离子的移动方向确定电极,电解饱和食盐水可以获得烧碱、氯气和氢气,根据电极反应确定溶液酸碱性的变化;
(2)金属的吸氧腐蚀中,正极上是氧气发生得电子的还原反应,负极上是金属失电子的氧化反应;
(3)在原电池的正极上发生得电子的还原反应,根据氧化还原反应的生成物来确定现象以及电极方程式.
(2)金属的吸氧腐蚀中,正极上是氧气发生得电子的还原反应,负极上是金属失电子的氧化反应;
(3)在原电池的正极上发生得电子的还原反应,根据氧化还原反应的生成物来确定现象以及电极方程式.
解答:
解:(1)阳离子交换膜法电解饱和食盐水(滴有酚酞)原理示意图,E口产生H2,则B极是阴极,A极是阳极,电解食盐水的离子方程式为:2Cl-+2H2O
Cl2↑+H2↑+2OH-,在阴极是氢离子得电子生成氢气的过程,所以B极区碱性增强,生成氢氧化钠,所以溶液变红色,故答案为:2Cl-+2H2O
Cl2↑+H2↑+2OH-;B;
(2)金属铁的吸氧腐蚀中,正极上是氧气发生得电子的还原反应O2+4e-+2H2O=4OH-,负极上是金属失电子的氧化反应Fe-2e-=Fe2+,故答案为:Fe-2e-=Fe2+;O2+4e-+2H2O=4OH-;
(3)向B杯中加入适量较浓的硫酸,发现G的指针向右偏移,“G是灵敏电流计,其指针总是偏向电源正极”所以所以说电子从C跑到D,即碘离子发生氧化反应,失去电子,生成碘单质遇到淀粉变蓝,是浓硫酸将低价的亚砷酸根离子氧化,该离子发生还原反应,实质是:AsO43-+2H++e-=AsO33-+H2O,
故答案为:溶液由无色变蓝色;AsO43-+2H++e-=AsO33-+H2O.
| ||
| ||
(2)金属铁的吸氧腐蚀中,正极上是氧气发生得电子的还原反应O2+4e-+2H2O=4OH-,负极上是金属失电子的氧化反应Fe-2e-=Fe2+,故答案为:Fe-2e-=Fe2+;O2+4e-+2H2O=4OH-;
(3)向B杯中加入适量较浓的硫酸,发现G的指针向右偏移,“G是灵敏电流计,其指针总是偏向电源正极”所以所以说电子从C跑到D,即碘离子发生氧化反应,失去电子,生成碘单质遇到淀粉变蓝,是浓硫酸将低价的亚砷酸根离子氧化,该离子发生还原反应,实质是:AsO43-+2H++e-=AsO33-+H2O,
故答案为:溶液由无色变蓝色;AsO43-+2H++e-=AsO33-+H2O.
点评:本题考查学生原电池的工作原理知识,难度不大,出题思路新颖,注意知识的归纳和整理是关键.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
下列反应中,属于氧化还原反应同时又是吸热反应的是( )
| A、Ba(OH)2?8H2O与NH4Cl反应 |
| B、铝与稀盐酸 |
| C、灼热的炭与水蒸气生成一氧化碳和氢气的反应 |
| D、煤与O2的燃烧反应 |