题目内容
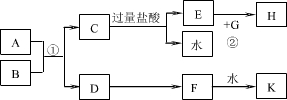
如图所示:已知A和E为金属单质,B是化合物且常温下为液态,F为两性化合物.按要求回答下列问题:
(1)E在元素周期表中位于第______周期;第______族.
(2)写出A和B反应的化学方程式:______.
(3)C和E反应的化学反应方程式为______.
解:B是化合物且常温下为液态,应为H2O,A为金属,和H2O在高温下发生反应,应为Fe和水的反应,则A为Fe,C为Fe3O4,和E在高温下发生反应生成F,F为两性化合物,应为Al2O3,E为Al,D为H2,
(1)E为Al,原子序数为13,原子核外有3个电子层,最外层电子数为3,则位于周期表第三周期ⅢA族,故答案为:三;ⅢA;
(2)Fe和H2O在高温下反应生成Fe3O4和H2,反应的方程式为3Fe+4 H2O(g) Fe3O4+4H2,故答案为:3Fe+4 H2O(g)
Fe3O4+4H2,故答案为:3Fe+4 H2O(g) Fe3O4+4H2;
Fe3O4+4H2;
(3)Al和Fe3O4在高温下发生铝热反应,反应的方程式为3Fe3O4+8Al 4Al2O3+9Fe,故答案为:3Fe3O4+8Al
4Al2O3+9Fe,故答案为:3Fe3O4+8Al 4Al2O3+9Fe.
4Al2O3+9Fe.
分析:B是化合物且常温下为液态,应为H2O,A为金属,和H2O在高温下发生反应,应为Fe和水的反应,则A为Fe,C为Fe3O4,和E在高温下发生反应生成F,F为两性化合物,应为Al2O3,E为Al,D为H2,结合物质的性质解答该题.
点评:本题考查无机物的推断,题目难度中等,本题注意在常温下为液态的化合物为H2O,注意把握相关物质的性质,牢固把握元素化合物知识是解答该类题目的前提.
(1)E为Al,原子序数为13,原子核外有3个电子层,最外层电子数为3,则位于周期表第三周期ⅢA族,故答案为:三;ⅢA;
(2)Fe和H2O在高温下反应生成Fe3O4和H2,反应的方程式为3Fe+4 H2O(g)
 Fe3O4+4H2,故答案为:3Fe+4 H2O(g)
Fe3O4+4H2,故答案为:3Fe+4 H2O(g) Fe3O4+4H2;
Fe3O4+4H2;(3)Al和Fe3O4在高温下发生铝热反应,反应的方程式为3Fe3O4+8Al
 4Al2O3+9Fe,故答案为:3Fe3O4+8Al
4Al2O3+9Fe,故答案为:3Fe3O4+8Al 4Al2O3+9Fe.
4Al2O3+9Fe.分析:B是化合物且常温下为液态,应为H2O,A为金属,和H2O在高温下发生反应,应为Fe和水的反应,则A为Fe,C为Fe3O4,和E在高温下发生反应生成F,F为两性化合物,应为Al2O3,E为Al,D为H2,结合物质的性质解答该题.
点评:本题考查无机物的推断,题目难度中等,本题注意在常温下为液态的化合物为H2O,注意把握相关物质的性质,牢固把握元素化合物知识是解答该类题目的前提.

练习册系列答案
相关题目