题目内容
5.a,b,c,d,e五种无色气体,进行如下实验:实验步聚 实验现象
①a,b相混合 气体变成棕色
②c,d相混合 产生白烟
③c,e分别通入少量溴水中 溴水均成无色透明溶液
④b,e分别通入氢硫酸中 都产生淡黄色的沉淀.
则a,b,c,d,e可能依次是( )
| A. | O2,NO,HCl,NH3,CO2 | B. | O2,NO,NH3,HCl,SO2 | ||
| C. | NO,O2,NH3,HCl,SO2 | D. | HBr,Cl2,NH3,H2S,C2H4 |
分析 a,b相混合气体变成棕色,说明生成NO2,a、b为NO、O2中的一种,b,e分别通入氢硫酸中都产生淡黄色的沉淀,则b、e都具有氧化性,则b为O2,a为NO,c,d相混合生成白烟,应生成氯化铵,c、d为NH3、HCl中的一种,c,e分别通入少量溴水中,可知c为NH3,d为HCl,以此解答该题.
解答 解:a,b相混合气体变成棕色,说明生成NO2,a、b为NO、O2中的一种,b,e分别通入氢硫酸中都产生淡黄色的沉淀,则b、e都具有氧化性,则b为O2,a为NO,c,d相混合生成白烟,应生成氯化铵,c、d为NH3、HCl中的一种,c,e分别通入少量溴水中,可知c为NH3,d为HCl,e与硫化氢反应生成硫,可为SO2,
则a,b,c,d,e可能依次是NO,O2,NH3,HCl,SO2,
故选C.
点评 本题考查无机物的推断,侧重于元素化合物知识的综合理解和运用的考查,为高频考点,有助于培养学生的分析能力和双基,注意把握常见气体的性质以及反应现象,难度不大.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
6.下列各组物质中所含分子数相同的是( )
| A. | 10g CO和10g N2 | B. | 10g C2H4和10g C3H6 | ||
| C. | 5.6L O2(标准状况)和0.5mol H2O | D. | 224mL He(标准状况)和1.6g CH4 |
3.在Al3++3H2O?Al(OH)3+3H+的平衡体系中,要抑制Al3+的水解,可采取的措施为( )
| A. | 加热 | B. | 加HCl | C. | 加NaOH | D. | 加AlCl3 |
10.下列溶液中,PH>7的是( )
| A. | CH3COONa | B. | NaCl | C. | NH4Cl | D. | AlCl3 |
14.纯净物X、Y、Z转化关系如图所示,下列判断正确的是( )
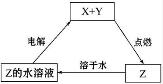

| A. | Z可能是氯化钠 | B. | Z可能是三氧化硫 | C. | X可能是金属铜 | D. | Y不可能是氢气 |
15.下列化合物的俗称与化学式不对应的是( )
| A. | 纯碱-Na2CO3 | B. | 熟石灰-Ca(OH)2 | ||
| C. | 明矾-Al2(SO4)3•12H2O | D. | 胆矾-CuSO4•5H2O |
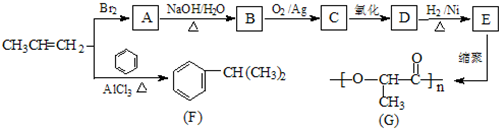
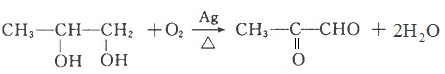 .
.