题目内容
6.有A、B、C三种元素,已知A的气态氢化物的分子式为H2A,A的气态氢化物的式量与A的最高价氧化物的式量之比为1:2.35.A的原子核内的质子数与中子数相等,B与A可形成离子化合物B2A,B+与A2-的电子层结构相同.C与A处于同一周期,C的单质为双原子分子,则(1)A的原子序数16.
(2)A为S,B为KC为Cl.
(3)B+离子结构示意图
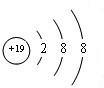 ,C原子的结构示意图为
,C原子的结构示意图为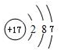 .
.(4)A、B、C三种元素最高价氧化物对应水化物的化学式为H2SO4、KOH、HClO4.它们酸性由强到弱的排列顺序是HClO4、H2SO4、KOH.
分析 有A、B、C三种元素,已知A的气态氢化物的分子式为H2A,则A的最高价有机物为AO3,A是氢化物的式量与A的最高价氧化物的式量之比为1:2.35,设A的相对分子质量为x,则(x+2):(x+48)=1:2.35,解得x=32,A的原子核内的质子数与中子数相等,则A的质子数为16,故A为S元素;B与A可形成离子化合物B2A,B+与A2-的电子层结构相同,则B为K元素;C与A(硫)处于同一周期,C的单质为双原子分子,则C为Cl.
解答 解:有A、B、C三种元素,已知A的气态氢化物的分子式为H2A,则A的最高价有机物为AO3,A是氢化物的式量与A的最高价氧化物的式量之比为1:2.35,设A的相对分子质量为x,则(x+2):(x+48)=1:2.35,解得x=32,A的原子核内的质子数与中子数相等,则A的质子数为16,故A为S元素;B与A可形成离子化合物B2A,B+与A2-的电子层结构相同,则B为K元素;C与A(硫)处于同一周期,C的单质为双原子分子,则C为Cl.
(1)由上述分析可知,A的质子数为16,则A的原子序数为16,
故答案为:16;
(2)由上述分析可知,A为S,B为K,C为Cl,
故答案为:S;K;Cl;
(3)K+离子结构示意图为 ,Cl原子的结构示意图为
,Cl原子的结构示意图为 ,
,
故答案为: ;
; ;
;
(4)A、B、C三种元素最高价氧化物对应水化物的化学式为H2SO4、KOH、HClO4,它们酸性由强到弱的排列顺序是:HClO4、H2SO4、KOH,
故答案为:H2SO4、KOH、HClO4;HClO4、H2SO4、KOH;
点评 本题考查结构性质位置关系应用,关键是计算确定A,侧重对元素周期律与化学用语的考查,比较基础.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
16.下列关于金刚石、石墨和C60的判断,正确的是( )
| A. | 均含共价键 | B. | 性质相同 | C. | 互为同位素 | D. | 互为同分异构体 |
14.某有机物的结构简式为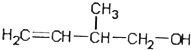 ,下列有关该物质叙述正确的是( )
,下列有关该物质叙述正确的是( )
 ,下列有关该物质叙述正确的是( )
,下列有关该物质叙述正确的是( )| A. | 不能与金属钠发生反应 | |
| B. | 不能使酸性高锰酸钾溶液褪色 | |
| C. | 在浓硫酸催化下.能与乙酸发生反应 | |
| D. | 常温下能与溴的四氯化碳溶液发生加成反应 |
11.现有下列短周期元素性质的数据:
试回答下列问题:
(1)上述元素中处于VA族的有:④⑦(用编号表示)
(2)处于第2周期的元素有:①③⑦⑧被称为“矾”的一类化合物中肯定含有表中①(以上均用编号表示)
(3)写出②、⑤的元素符号:Mg、Cl.
(4)上述元素中金属性最强的是:Na(用元素符号表示)
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)上述元素中处于VA族的有:④⑦(用编号表示)
(2)处于第2周期的元素有:①③⑦⑧被称为“矾”的一类化合物中肯定含有表中①(以上均用编号表示)
(3)写出②、⑤的元素符号:Mg、Cl.
(4)上述元素中金属性最强的是:Na(用元素符号表示)
4.下列化合物分子,在核磁共振氢谱图中能给出三种信号峰的是( )
| A. | CH3CH2CH3 | B. | CH3-O-CH3 | C. | 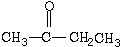 | D. | 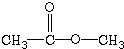 |
2.绿矾(FeSO4•7H2O)是治疗缺铁性贫血药品中的重要成分.下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
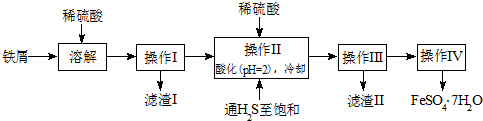
已知:室温下饱和H2S溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.
请回答下列问题:
(一)绿矾的制备
(1)检验制得的绿矾中是否含有Fe3+的实验操作是取少量溶于水配成溶液,滴加1~2滴KSCN溶液,振荡,若变为红色溶液则含有Fe3+,否则不含Fe3+.
(2)操作II中,通入硫化氢至饱和的目的是把Fe3+还原成Fe2+,除去溶液中的Sn2+,并防止Fe2+被氧化;在溶液中用硫酸酸化至pH=2的目的是防止Fe2+生成沉淀.
(3)操作IV的顺序依次为:蒸发浓缩、冷却结晶、过滤洗涤.
(二)绿矾中FeSO4•7H2O含量的测定
若用容量法测定绿矾中FeSO4•7H2O的含量.滴定反应是:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O
实验方案如下:
①称取15.041g绿矾产品,溶解,在250mL容量瓶中定容.
②量取25.00mL待测溶液于锥形瓶中.
③用0.0500mol/L KMnO4溶液(硫酸酸化)滴定至终点,记录初读数和末读数.
④重复操作②③1~2次或做平行实验1~2次.
⑤数据处理.
(4)上述实验方案中的步骤④是重复操作②③1~2次或做平行实验1~2次.
(5)洁净的滴定管在滴定前必须进行的操作有:
①检验活塞是否漏水;②用蒸馏水洗涤2~3次,再用高锰酸钾标准溶液润洗滴定管2~3次;
③向滴定管中加入KMnO4标准溶液到0刻度以上,赶走尖嘴部位的气泡,调液面至0或0刻度线以下,初读数.
(三)数据处理
某小组同学的实验数据记录如下:(FeSO4•7H2O的摩尔质量为278g/mol)
(6)上述样品中FeSO4•7H2O的质量分数为0.975(用小数表示,保留三位小数).

已知:室温下饱和H2S溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.
请回答下列问题:
(一)绿矾的制备
(1)检验制得的绿矾中是否含有Fe3+的实验操作是取少量溶于水配成溶液,滴加1~2滴KSCN溶液,振荡,若变为红色溶液则含有Fe3+,否则不含Fe3+.
(2)操作II中,通入硫化氢至饱和的目的是把Fe3+还原成Fe2+,除去溶液中的Sn2+,并防止Fe2+被氧化;在溶液中用硫酸酸化至pH=2的目的是防止Fe2+生成沉淀.
(3)操作IV的顺序依次为:蒸发浓缩、冷却结晶、过滤洗涤.
(二)绿矾中FeSO4•7H2O含量的测定
若用容量法测定绿矾中FeSO4•7H2O的含量.滴定反应是:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O
实验方案如下:
①称取15.041g绿矾产品,溶解,在250mL容量瓶中定容.
②量取25.00mL待测溶液于锥形瓶中.
③用0.0500mol/L KMnO4溶液(硫酸酸化)滴定至终点,记录初读数和末读数.
④重复操作②③1~2次或做平行实验1~2次.
⑤数据处理.
(4)上述实验方案中的步骤④是重复操作②③1~2次或做平行实验1~2次.
(5)洁净的滴定管在滴定前必须进行的操作有:
①检验活塞是否漏水;②用蒸馏水洗涤2~3次,再用高锰酸钾标准溶液润洗滴定管2~3次;
③向滴定管中加入KMnO4标准溶液到0刻度以上,赶走尖嘴部位的气泡,调液面至0或0刻度线以下,初读数.
(三)数据处理
某小组同学的实验数据记录如下:(FeSO4•7H2O的摩尔质量为278g/mol)
| 实验次数 | 初读数(mL) | 末读数(mL) |
| 1 | 0.20 | 21.40 |
| 2 | 0.00 | 21.00 |
| 3 | 1.60 | 26.60 |