题目内容
13.以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下: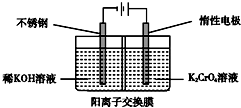
下列说法不正确的是( )
| A. | 在阴极室,发生的电极反应为2H2O+2e-═2OH-+H2↑ | |
| B. | 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+?Cr2O72-+H2O向右移动 | |
| C. | 该制备过程中总反应的化学方程式为4K2CrO4+4H2O$\frac{\underline{\;通电\;}}{\;}$2K2Cr2O7+4KOH+2H2↑+O2↑ | |
| D. | 测定阳极液中K和Cr的含量,若K与Cr的物质的量之比(nK/nCr)为d,则此时铬酸钾的转化率为1 |
分析 A、阴极上得电子发生还原反应;
B、阳极上水失电子生成氧气和氢离子,氢离子浓度增大导致平衡移动,根据氢离子浓度的变化判断溶液颜色的变化;
C、电解时,铬酸钾和水放电生成重铬酸钾、氢气、氧气和氢氧化钠;
D、根据原子守恒计算其转化率.
解答 解:A、根据题意可知:电极均为惰性电极,在阴极室,水得电子变成氢气,电极反应为:2H2O+2e-=2OH-+H2↑,故A正确;
B、阳极室水失去电子,电极反应为:2H2O-4e-=4H++O2↑,使阳极区氢离子浓度增大,平衡右移,故B正确;
C、总制备方程式为4K2CrO4 +4H2O $\frac{\underline{\;通电\;}}{\;}$2K2Cr2O7 +4KOH+2H2↑+O2↑,故C正确;
D、设加入反应容器内的K2CrO4为1mol,反应过程中有xmol K2CrO4转化为K2Cr2O7,则阳极区剩余K2CrO4为(1-x)mol,对应的n(K)=2(1-x)mol,n(Cr)=(1-x)mol,生成的K2Cr2O7为$\frac{x}{2}$mol,对应的n(K)=xmol,n(Cr)=xmol,根据:K与Cr的物质的量之比为d,解得x=2-d,转化率为$\frac{2-d}{1}$=2-d,故D错误;
故选D.
点评 本题考查了电解原理,难点是计算转化率,根据原子守恒即可计算其转化率,根据阴阳极上发生的反应类型写出相应的电极反应式.

练习册系列答案
相关题目
3.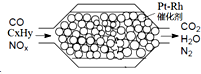 汽车尾气含氮氧化物(NOX)、碳氢化合物(CXHY)、碳等,直接排放容易造成“雾霾”.因此,不少汽车都安装尾气净化装置(净化处理过程如图).下列有关叙述,错误的是( )
汽车尾气含氮氧化物(NOX)、碳氢化合物(CXHY)、碳等,直接排放容易造成“雾霾”.因此,不少汽车都安装尾气净化装置(净化处理过程如图).下列有关叙述,错误的是( )
 汽车尾气含氮氧化物(NOX)、碳氢化合物(CXHY)、碳等,直接排放容易造成“雾霾”.因此,不少汽车都安装尾气净化装置(净化处理过程如图).下列有关叙述,错误的是( )
汽车尾气含氮氧化物(NOX)、碳氢化合物(CXHY)、碳等,直接排放容易造成“雾霾”.因此,不少汽车都安装尾气净化装置(净化处理过程如图).下列有关叙述,错误的是( )| A. | 尾气造成“雾霾”与汽油未充分燃烧有关 | |
| B. | 尾气处理过程,氮氧化物(NOX)被还原 | |
| C. | Pt-Rh催化剂可提高尾气净化反应的平衡转化率 | |
| D. | 使用氢氧燃料电池作汽车动力能有效控制雾霾 |
4.如图是一种微生物燃料电池的原理示意图.下列有关该微生物燃料电池的说法正确的是( ) 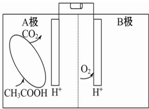

| A. | A极为正极,B极为负极 | |
| B. | 电池内电解质溶液中所含的H+由B极移向A极 | |
| C. | A极的电极反应为:CH3COOH-8e-+2H2O═2CO2↑+8H+ | |
| D. | 电池工作过程中,电解质溶液的pH会明显下降 |
1.下列实验操作正确的是( )


| A. | 用图1示装置制备Cl2 | |
| B. | 将混合气体通过装有NaOH溶液的洗气瓶除去Cl2中混有的HCl | |
| C. | 用图2示装置分离CH3COOC2H5与饱和Na2CO3溶液 | |
| D. | 称取1.06 g Na2CO3固体,置于100 mL容量瓶中,加水稀释,配制0.10 mol•L-1的Na2CO3溶液 |
18.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,11.2L苯中含有C-H键的数目为3NA | |
| B. | 常温下,1.0L pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| C. | 常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 | |
| D. | 标准状况下22.4LSO3中含有的氧原子数目为3NA |
5. A1/MnO4-电池是一种高能电池,以Ga2O3为缓蚀剂,其示意图如图所示.已知电池总反应为Al+MnO4-+2H2O═Al(OH)4-+MnO2.下列说法正确的是( )
A1/MnO4-电池是一种高能电池,以Ga2O3为缓蚀剂,其示意图如图所示.已知电池总反应为Al+MnO4-+2H2O═Al(OH)4-+MnO2.下列说法正确的是( )
 A1/MnO4-电池是一种高能电池,以Ga2O3为缓蚀剂,其示意图如图所示.已知电池总反应为Al+MnO4-+2H2O═Al(OH)4-+MnO2.下列说法正确的是( )
A1/MnO4-电池是一种高能电池,以Ga2O3为缓蚀剂,其示意图如图所示.已知电池总反应为Al+MnO4-+2H2O═Al(OH)4-+MnO2.下列说法正确的是( )| A. | 电池工作时,K+向负极移动 | |
| B. | 电池工作时,Al电极周围溶液pH增大 | |
| C. | 正极反应为MnO4-+2H2O+3e-═MnO2+4OH- | |
| D. | 电池工作时,电子由Al经溶液流向Ni |
2.下列除去杂质的方法正确的是(括号内的是杂质)( )
| A. | N2(CO):通过灼热的CuO粉末 | B. | Na2SO4溶液(Na2CO3):加盐酸 | ||
| C. | NaCl(NH4Cl):加热 | D. | NO2(NO):通入水中 |
3.我国预计在2020年前后建成自己的载人空间站.为了实现空间站的零排放,循环利用人体呼出的C02并提供02,我国科学家设计了一种装置(如图),实现了“太阳能一电能一化学能”转化,总反应方程式为2C02=2C0+02.关于该装置的下列说法正确的是( )
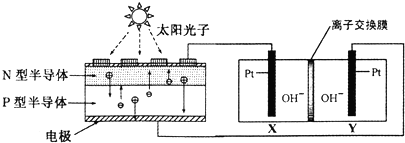

| A. | 图中N型半导体为正极,P型半导体为负极 | |
| B. | 图中离子交换膜为阳离子交换膜 | |
| C. | 反应完毕,该装置中电解质溶液的碱性增强 | |
| D. | 人体呼出的气体参与X电极的反应:CO2+2e一+H2O═CO+2OH- |

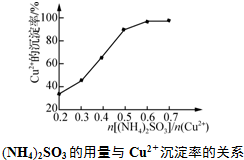 ,工业上$\frac{n[(N{H}_{4})_{2}S{O}_{3}]}{n(C{u}^{2+})}$采用0.6最为适宜,此时(NH4)2SO3略过量,其原因是保证生成的CuCl不被氧气氧化或(NH4)2SO3被空气中的氧气氧化.
,工业上$\frac{n[(N{H}_{4})_{2}S{O}_{3}]}{n(C{u}^{2+})}$采用0.6最为适宜,此时(NH4)2SO3略过量,其原因是保证生成的CuCl不被氧气氧化或(NH4)2SO3被空气中的氧气氧化.