题目内容
将等质量的两份锌粉a、b分别加入到足量的稀硫酸,同时向a中加少量CuSO4溶液,下图中产生H2的体积V(L)与时间t(min)的关系,其中正确的是( )
A、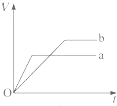 |
B、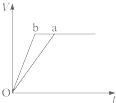 |
C、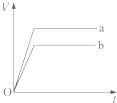 |
D、 |
考点:化学反应速率的影响因素,化学方程式的有关计算
专题:
分析:锌和硫酸反应,加入硫酸铜,会置换出金属铜,形成锌、铜、稀硫酸原电池,加速金属锌和硫酸反应的速率,产生氢气的量取决于金属锌的质量,以此解答.
解答:
解:锌和硫酸反应,加入硫酸铜,会置换出金属铜,形成锌、铜、稀硫酸原电池,加速金属铁和硫酸反应的速率,所以反应速率是:a>b,速率越大,锌完全反应时所用的时间越短,所以a所用的时间小于b的时间;产生氢气的量取决于金属锌的质量,而a中,金属锌一部分用于置换金属铜,导致和硫酸反应生成氢气的量减少,所以氢气的体积是:a<b.
故选A.
故选A.
点评:本题考查化学反应速率的影响因素,为高考高频考点,侧重于学生的分析能力的考查,注意原电池反应的特点以及稀硫酸过量的信息,难度不大.

练习册系列答案
相关题目
下列表示对应化学反应的离子方程式正确的是( )
| A、向氯化铝溶液通入过量的氨气:Al3++4OH-═AlO2-+2H2O |
| B、过量氯气通入溴化亚铁溶液中2Cl2+2Fe2++2Br-═4Cl-+2Fe3++Br2 |
| C、次氯酸钠与浓盐酸反应产生Cl2:ClO-+Cl-+H2O=Cl2↑+2OH- |
| D、NaHCO3溶液与少量Ba(OH)2溶液反应:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O |
在给定条件下,下列加点的物质在化学反应中能被完全消耗的是( )
A、用50 mL 8 mol?L-1
| ||||||
B、标准状况下,1 g铝片投入20 mL 18.4 mol?L-1的
| ||||||
C、向100 mL 3 mol?L-1的
| ||||||
D、在5×107 Pa、500℃和铁触媒催化的条件下,用28g
|
下列各组离子能在水溶液中大量共存的是( )
| A、H+、Fe2+、ClO-、SO42- |
| B、Na+、Cu2+、S2-、ClO- |
| C、Na+、Ba2+、OH-、NO3- |
| D、Na+、Al3+、SiO32-、CO32- |
下列事实,不能用勒夏特列原理解释的是( )
| A、在溴水中存在如下平衡:Br2+H2O?HBr+HBrO 当加入NaOH溶液后颜色变浅 |
| B、对2HI?H2+I2(g)平衡体系增加压强使颜色变深 |
| C、反应CO+NO2?CO2+NO△H<0 升高温度使平衡向逆方向移动 |
| D、合成氨反应:N2+3H2?2NH3,△H<0 为使氨的产率提高,理论上应采取低温高压的措施 |
 铝和氢氧化钾都是重要的工业产品.请回答:
铝和氢氧化钾都是重要的工业产品.请回答: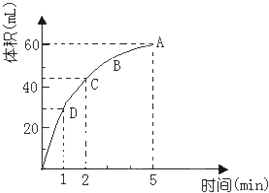 为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于50mL密度为1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示.请依图回答下列问题:
为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于50mL密度为1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示.请依图回答下列问题: