题目内容
下列关于周期表的说法正确的是( )
| A、同一周期元素原子的最外层电子数相同 |
| B、同一主族元素原子的电子层数相同 |
| C、能生成碱的金属都在第ⅠA族 |
| D、第ⅦA族元素统称为卤族元素 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:A、电子层数相同的元素在同一周期;
B、最外层电子数相同的元素在同一主族;
C、第IIA、IIIA也含有金属元素;
D、第ⅦA族元素统称为卤族元素.
B、最外层电子数相同的元素在同一主族;
C、第IIA、IIIA也含有金属元素;
D、第ⅦA族元素统称为卤族元素.
解答:
解:A、在周期表中,把电子层数相同的元素放在一个橫行中称为周期,所以同一周期元素原子的最外层电子数相同,故A错误;
B、元素性质相似,最外层电子数相同的元素在同一主族,故B错误;
C、第IIA、IIIA也含有金属元素,如第IIA的镁元素属于金属元素,能生成碱,故C错误;
D、第ⅦA族元素包括F、Cl、Br、I、At等元素统称为卤族元素,故D正确.
故选D.
B、元素性质相似,最外层电子数相同的元素在同一主族,故B错误;
C、第IIA、IIIA也含有金属元素,如第IIA的镁元素属于金属元素,能生成碱,故C错误;
D、第ⅦA族元素包括F、Cl、Br、I、At等元素统称为卤族元素,故D正确.
故选D.
点评:本题考查结构性质位置关系,比较基础,注意元素周期律的理解掌握,注意识记周期表中一些特殊性.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
下列装置中四块相同的Zn片,放置一段时间后腐蚀速率由慢到快的顺序是( )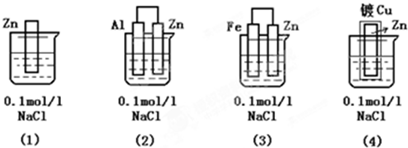

| A、①②③④ | B、④②①③ |
| C、③①②④ | D、②①③④ |
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )| A、该硫酸的物质的量浓度为9.2 mol/L |
| B、若该硫酸与等体积的水混合,所得溶液的质量分数小于49% |
| C、若实验室需要4.6 mol/L的稀硫酸480 mL,则应用量筒量取该硫酸125.0mL |
| D、等质量的水与该硫酸混合所得溶液的物质的量浓度大于9.2 mol/L |
某反应A(g)+3B(g)═2C(g),以下反应速率的表示中最快的是( )
| A、VA=0.4 mol/(L?S) |
| B、VB=0.8 mol/(L?S) |
| C、Vc=0.6 mol/(L?S) |
| D、无法比较 |
一支25mL滴定管,内盛溶液液面在15.00mL刻度处,当将滴定管内液体全部排出时,所得液体的体积是( )
| A、10.00mL |
| B、15.00mL |
| C、小于10.00mL |
| D、大于10.00mL |