题目内容
在一定温度下,10L密闭容器中加入5.0molSO2、4.5molO2,发生反应:2SO2+O2?2SO3经10min后反应达平衡时O2的浓度为0.30mol/L.请计算(写出计算过程):
(1)10min内SO2的转化率;
(2)平衡常数K.
(1)10min内SO2的转化率;
(2)平衡常数K.
考点:化学平衡的计算
专题:化学平衡专题
分析:10L密闭容器中加入5.0molSO2、4.5molO2,c(SO2)=0.50mol/L,c(O2)=0.45mol/L,经10min后反应达平衡时O2的浓度为0.30mol/L,
则 2SO2+O2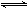 2SO3
2SO3
起始浓度(mol/L) 0.50 0.45 0
变化浓度(mol/L) 0.30 0.15 0.30
平衡浓度(mol/L) 0.20 0.30 0.30
(1)利用反应的浓度和起始浓度计算转化率;
(2)K为生成物浓度幂之积与反应物浓度幂之积的比.
则 2SO2+O2
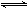 2SO3
2SO3起始浓度(mol/L) 0.50 0.45 0
变化浓度(mol/L) 0.30 0.15 0.30
平衡浓度(mol/L) 0.20 0.30 0.30
(1)利用反应的浓度和起始浓度计算转化率;
(2)K为生成物浓度幂之积与反应物浓度幂之积的比.
解答:
解:10L密闭容器中加入5.0molSO2、4.5molO2,c(SO2)=0.50mol/L,c(O2)=0.45mol/L,经10min后反应达平衡时O2的浓度为0.30mol/L,
则 2SO2+O2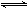 2SO3
2SO3
起始浓度(mol/L) 0.50 0.45 0
变化浓度(mol/L) 0.30 0.15 0.30
平衡浓度(mol/L) 0.20 0.30 0.30
(1)10min内SO2的转化率为
×100%=60%,答:10min内SO2的转化率为60%;
(2)平衡常数K=
=
=7.5L/mol,答:平衡常数K为7.5L/mol.
则 2SO2+O2
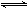 2SO3
2SO3起始浓度(mol/L) 0.50 0.45 0
变化浓度(mol/L) 0.30 0.15 0.30
平衡浓度(mol/L) 0.20 0.30 0.30
(1)10min内SO2的转化率为
| 0.3mol/L |
| 0.5mol/L |
(2)平衡常数K=
| c(SO 3) 2 |
| c(O 2)×c(SO 2) 2 |
| (0.3mol/L) 2 |
| (0.2mol/L) 2×0.3mol/L |
点评:本题考查化学平衡的计算,明确化学平衡的三段法计算格式及平衡常数的计算方法是解答本题的关键,注意利用平衡浓度计算平衡常数,题目难度中等.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
下列说法不正确的是( )
| A、Ksp只与难溶电解质的性质和温度有关 |
| B、由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀 |
| C、任意两种难溶电解质作比较时,Ksp小的,溶解度一定小 |
| D、t℃时,Ksp(CaCO3)=4×10-16,则CaCO3饱和溶液中c(Ca2+)=2×10-8 mol/L |
下列各式属于正确的水解反应的离子方程式的是( )
| A、HCO3-+H2O?CO32-+H3O+ |
| B、S2-+H2O?H2S+2OH- |
| C、Fe3++3H2O?Fe(OH)3+3H+ |
| D、CH3COOH+OH-?CH3COO-+H2O |
加水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是( )
A、
| ||
B、
| ||
| C、c(H+)?c(OH-) | ||
| D、n(OH-) |
硬铝合金包括Al-Cu-Mg系和Al-Cu-Mn系合金,广泛用于现代社会.下面关于硬铝的说法,错误的是( )
| A、强度跟铝相比有很大的提高,在某些性能上相当于钢材 |
| B、密度较小,只有钢材的三分之一左右,适用于做飞行器、火箭、卫星、导弹等 |
| C、熔点和铝相比有一定的提高,常被用于制造家庭使用的炊具 |
| D、抗腐蚀性能较强,常被建筑行业用作材料以及门窗框架 |
下列说法不正确的是( )
| A、浓硫酸能与铜反应释放出氢气 |
| B、浓硫酸能与灼热的木炭反应,生成二氧化碳和二氧化硫 |
| C、浓硫酸具有吸水性,在实验中常用作干燥剂 |
| D、冷的浓硫酸可以用铁质或铝质容器储存 |
下列三种化合物由左到右是按强电解质、弱电解质、非电解质的顺序排列的一组是( )
| A、HCl、CaCO3、SO2 |
| B、KNO3、CH3COOH、NH3 |
| C、HClO、H2S、C2H5OH |
| D、BaSO4、H3PO4、H2O |
下列过程或事实不涉及氧化还原反应的是( )
①蔗糖炭化
②用氢氟酸雕刻玻璃
③铁遇冷的浓硫酸钝化
④装碱液的试剂瓶不用玻璃塞
⑤雷雨发庄稼
⑥浓硝酸常显黄色.
①蔗糖炭化
②用氢氟酸雕刻玻璃
③铁遇冷的浓硫酸钝化
④装碱液的试剂瓶不用玻璃塞
⑤雷雨发庄稼
⑥浓硝酸常显黄色.
| A、①③⑤⑥ | B、②④ |
| C、②④⑥ | D、①②③④⑤⑥ |