题目内容
8.一定量的硝酸与 3.2g 铜充分反应,得到的还原产物有NO2和NO.反应后溶液中含有a mol H+,则此时溶液中含有NO3- 的物质的量是( )| A. | a mol | B. | (a+0.1)mol | C. | 0.05 mol | D. | 无法计算 |
分析 反应后氢离子有剩余,说明硝酸过量,铜完全反应,反应后溶液中的溶质是硝酸和硝酸铜,根据硝酸中NO3-和H+、硝酸铜中NO3-和Cu2+的关系式计算出NO3-的物质的量.
解答 解:3.2g的物质的量为:$\frac{3.2g}{64g/mol}$=0.05mol,反应后溶液中含有a mol H+,说明硝酸过量,根据Cu(NO3)2~Cu2+~C u~2NO3-可知,硝酸铜中含有NO3-的物质的量为:n(NO3-)=2n(Cu2+)=0.05mol×2=0.1mol,
氢离子主要来自硝酸,根据关系式HNO3~H+~NO3-可知,H+对应的NO3-的物质的量为:n(NO3-)=n(H+)=amol,
所以此时溶液中含有NO3-的物质的量为:0.1mol+amol=(0.1+a )mol,
故选B.
点评 本题考查了物质的量的计算,题目难度不大,明确发生反应的实质为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
18.针对下面10种元素,完成以下各小题.
(1)地壳中含量最多的元素是氧(填名称).
(2)Mg的原子结构示意图为 .
.
(3)化学性质最不活泼的元素是Ne(填元素符号).
(4)MgO和Al2O3中,属于两性氧化物的是Al2O3.
(5)H2S和HCl相比,稳定性较强的是HCl.
(6)N与O相比,原子半径较小的是O.
(7)最高价氧化物对应的水化物中碱性最强的是NaOH(填化学式).
(8)可用来制造光导纤维的物质是SiO2,晶体硅的主要用途是作半导体材料(写出一种).
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)Mg的原子结构示意图为
 .
.(3)化学性质最不活泼的元素是Ne(填元素符号).
(4)MgO和Al2O3中,属于两性氧化物的是Al2O3.
(5)H2S和HCl相比,稳定性较强的是HCl.
(6)N与O相比,原子半径较小的是O.
(7)最高价氧化物对应的水化物中碱性最强的是NaOH(填化学式).
(8)可用来制造光导纤维的物质是SiO2,晶体硅的主要用途是作半导体材料(写出一种).
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
19.下列有机反应中,有一种反应类型与其他三种反应类型不同的是( )
| A. | CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$ CH3COOCH2CH3+H2O | |
| B. | 2CH3CH2OH+O2 $→_{△}^{催化剂}$ 2CH3CHO+2H2O | |
| C. | CH4+Cl2 $\stackrel{光照}{→}$ CH3Cl+HCl | |
| D. | 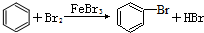 |
16.向纯水中加入少量H2SO4,当温度不变时,该溶液中增大的量是( )
| A. | c(OH-) | B. | c(H+) | ||
| C. | c(OH-) 与 c(H+) 的乘积 | D. | 水电离出的 c(H+) |
13.下列各组物质充分反应后,再滴入 KSCN 溶液,显红色的是( )
| A. | 足量氯水与 FeCl2 溶液 | B. | 足量铁与稀盐酸 | ||
| C. | 足量铁粉与CuCl2 溶液 | D. | 足量铁粉与 FeCl3 溶液 |
18.某化合物有碳、氢、氧三种元素组成,其红外光谱图有C-H键、O-H键、C-O键的振动吸收,该有机物的相对分子质量是60,则该有机物的结构简式是( )
| A. | CH3CH2OCH3 | B. | CH3CH(OH)CH3 | C. | CH3CH2COOH | D. | CH3CH2CHO |
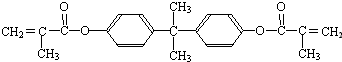
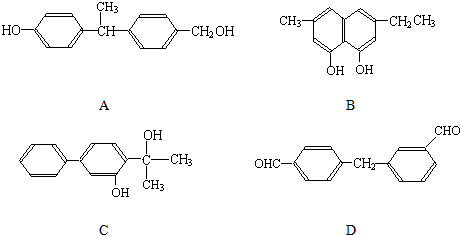
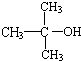 结构相似的醇不能被氧化为醛或酸.
结构相似的醇不能被氧化为醛或酸.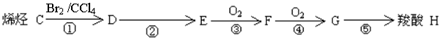
 .
. .
. .
.