题目内容
氧化还原反应中实际上包含氧化和还原两个过程.下面是一个还原过程的反应式:NO3-+4H++3e-→NO+2H2O.在KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中,有一种物质(甲)能使上述还原过程发生.
(1)该物质是
(2)写出并配平该氧化还原反应的方程式:
(3)反应中硝酸体现了 、 性质.
(4)反应中若产生0.2mol气体,则转移电子的物质的量是 mol.
(1)该物质是
(2)写出并配平该氧化还原反应的方程式:
(3)反应中硝酸体现了
(4)反应中若产生0.2mol气体,则转移电子的物质的量是
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)还原过程中N元素的化合价降低,则应与还原剂Cu2O发生氧化还原反应;
(2)根据物质中的元素的化合价处于低价时具有还原性,再根据电子守恒及质量守恒定律来配平化学反应方程式;
(3)反应生成硝酸铜、NO,生成硝酸盐体现酸性,生成NO时N元素的化合价降低;
(4)该反应生成的气体为NO,然后利用化合价变化分析转移的电子数.
(2)根据物质中的元素的化合价处于低价时具有还原性,再根据电子守恒及质量守恒定律来配平化学反应方程式;
(3)反应生成硝酸铜、NO,生成硝酸盐体现酸性,生成NO时N元素的化合价降低;
(4)该反应生成的气体为NO,然后利用化合价变化分析转移的电子数.
解答:
解:(1)还原过程的反应式为NO3-+4H++3e--→NO+2H2O,则具有还原性的物质可使还原反应发生,只有Cu2O符合,Cu元素的化合价升高,故答案为:Cu2O;
(2)KMnO4、Na2CO3、Fe2(SO4)3中Mn、C、Fe元素都处在最高价,则具有氧化性,只有Cu2O中Cu处在较低价,则具有还原性,在NO3-+4H++3e→NO+2H2O中发生的氧化剂被还原的反应,则该氧化还原反应为Cu2O+HNO3→NO↑+Cu(NO3)2+H2O,Cu元素由+1价升高到+2价,N元素由+5价降低到+2价,由电子守恒及质量守恒定律,配平的化学反应为3Cu2O+14HNO3═2NO↑+6Cu(NO3)2+7H2O,故答案为:3Cu2O+14HNO3═2NO↑+6Cu(NO3)2+7H2O;
(3)因硝酸中的N元素的化合价为+5价,NO中N元素的化合价为+2价,在该反应中N元素的化合价降低,则体现硝酸的氧化性,而硝酸与硝酸中N元素的化合价相同,则体现硝酸具有酸性,故答案为:氧化性;酸性;
(4)若产生0.2mol气体,则转移电子为0.2mol×(5-2)=0.6mol,故答案为:0.6.
(2)KMnO4、Na2CO3、Fe2(SO4)3中Mn、C、Fe元素都处在最高价,则具有氧化性,只有Cu2O中Cu处在较低价,则具有还原性,在NO3-+4H++3e→NO+2H2O中发生的氧化剂被还原的反应,则该氧化还原反应为Cu2O+HNO3→NO↑+Cu(NO3)2+H2O,Cu元素由+1价升高到+2价,N元素由+5价降低到+2价,由电子守恒及质量守恒定律,配平的化学反应为3Cu2O+14HNO3═2NO↑+6Cu(NO3)2+7H2O,故答案为:3Cu2O+14HNO3═2NO↑+6Cu(NO3)2+7H2O;
(3)因硝酸中的N元素的化合价为+5价,NO中N元素的化合价为+2价,在该反应中N元素的化合价降低,则体现硝酸的氧化性,而硝酸与硝酸中N元素的化合价相同,则体现硝酸具有酸性,故答案为:氧化性;酸性;
(4)若产生0.2mol气体,则转移电子为0.2mol×(5-2)=0.6mol,故答案为:0.6.
点评:本题考查氧化还原反应,为高考常见题型,注意把握元素的化合价及反应中的变化为解答的关键,侧重基本概念和转移电子数的考查,题目难度不大.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
下列事实(常温下)不能说明醋酸是弱电解质的是( )
| A、醋酸钠溶液pH>7 |
| B、醋酸溶液能溶解碳酸钙 |
| C、0.1mol?L-1醋酸溶液pH=2.9 |
| D、pH=1的醋酸溶液稀释100倍后pH<3 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol Cl2与过量的镁铁反应,转移2NA个电子 |
| B、常温下,16g CH4含有8NA个电子 |
| C、1L 0.5mol?L-1 Na2SO4溶液中含有NA个SO42- |
| D、常温常压下,22.4L CO2含有NA个CO2分子 |
 试回答:
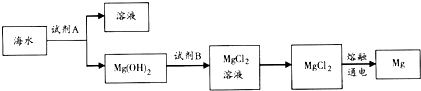
试回答: 利用海洋资源可以获得很多物质,如从海水得到的食盐水可以用来制取食盐,可以用来电解得到许多化工原料,可以通过蒸馏获得淡水等.
利用海洋资源可以获得很多物质,如从海水得到的食盐水可以用来制取食盐,可以用来电解得到许多化工原料,可以通过蒸馏获得淡水等.