题目内容
8.已知25℃时,AgCl的Ksp=1.8×10-10,下列说法正确的是( )| A. | 在一定温度下AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数 | |
| B. | 在任何含AgCl固体的溶液中都存在c(Ag+)=c(Cl-) | |
| C. | 向饱和AgCl水溶液中加入盐酸,其Ksp值变大 | |
| D. | 将足量AgCl固体投入100mL0.1mol/L MgCl2溶液充分搅拌后冷却到25℃时,此时c(Ag+)=9×10-10mol/L |
分析 A.AgCl的饱和溶液中Ksp=c(Ag+)c(Cl-);
B.在盐酸或硝酸银可抑制AgCl的溶解;
C.Ksp只与温度有关;
D.c(Cl-)=0.2mol/L,c(Ag+)=$\frac{Ksp}{c(C{l}^{-})}$.
解答 解:A.AgCl的饱和溶液中Ksp=c(Ag+)c(Cl-),若不饱和,则Ag+和Cl-浓度的乘积不一定是一个常数,故A错误;
B.在盐酸或硝酸银可抑制AgCl的溶解,则溶液中不一定存在c(Ag+)=c(Cl-),故B错误;
C.Ksp只与温度有关,则向饱和AgCl水溶液中加入盐酸,其Ksp值不变,故C错误;
D.c(Cl-)=0.2mol/L,c(Ag+)=$\frac{Ksp}{c(C{l}^{-})}$=$\frac{1.8×1{0}^{-10}}{0.2}$=9×10-10mol/L,故D正确;
故选D.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握溶解平衡、Ksp的计算为解答的关键,侧重分析与应用能力的考查,注意选项A为易错点,题目难度不大.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
18.以NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 在标准状况下,NA个H2O 分子所占体积约为22.4L | |
| B. | 0.1 mol H2、0.2 mol O2、0.3 mol N2和0.4 mol CO2组成的混合气体在标准状况下的体积约为22.4 L | |
| C. | 常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1 NA | |
| D. | 0.5mol/L的NaCl溶液中Cl-的个数为是0.5NA |
16.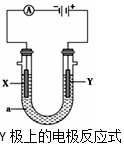 电解原理在化学工业中有广泛应用.根据如图装置,回答以下问题:
电解原理在化学工业中有广泛应用.根据如图装置,回答以下问题:
(1)若X、Y都是惰性电极,a是硫酸钠溶液,实验开始时,同时在两边各滴入几滴石蕊试剂,一段时间后,在X极附近观察到的现象是溶液变蓝、产生气泡,Y极上的电极反应式为4OH--4e-=2H2O+O2↑.
(2)若X、Y都是惰性电极,a是CuSO4溶液,电解一段时间后,阳极上产生气体的体积为0.224L(标准状况下),则阴极上析出金属的质量为1.28g;
(3)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是D (填序号).
 电解原理在化学工业中有广泛应用.根据如图装置,回答以下问题:
电解原理在化学工业中有广泛应用.根据如图装置,回答以下问题:(1)若X、Y都是惰性电极,a是硫酸钠溶液,实验开始时,同时在两边各滴入几滴石蕊试剂,一段时间后,在X极附近观察到的现象是溶液变蓝、产生气泡,Y极上的电极反应式为4OH--4e-=2H2O+O2↑.
(2)若X、Y都是惰性电极,a是CuSO4溶液,电解一段时间后,阳极上产生气体的体积为0.224L(标准状况下),则阴极上析出金属的质量为1.28g;
(3)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是D (填序号).
| 方案 | X | Y | a溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 | AgNO3 |
| C | 铁 | 银 | Fe(NO3)3 |
| D | 铁 | 银 | AgNO3 |
3.下列反应中反应物键能总和高于生成物键能总和的是( )
| A. | 碳酸钙受热分解 | B. | 乙醇的燃烧 | ||
| C. | 铝粉与氧化铁粉末反应 | D. | 氧化钙与水反应 |
13.化学与人类生产、生活、社会可持续发展密切相关.下列有关说法不正确的是( )
| A. | MgO和Al2O3在工业上用于制作耐高温材料,也可用于电解法冶炼Mg、Al | |
| B. | 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质 | |
| C. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” | |
| D. | 高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,既能杀菌消毒又能净水 |
20.在P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平)的反应中,3.75mol CuSO4可氧化P的物质的量为( )mol?.生成2mol Cu3P 时,参加反应的P的物质的量为( ) mol?
| A. | 0.75,2.2 | B. | 1.5,2.2 | C. | 0.75,4.4 | D. | 1.5,4.4 |
17.在某无色透明的酸性溶液中,能共存的离子组是( )
| A. | Na+、K+、SO4 2-、HCO3 - | B. | Cu2+、K+、SO4 2-、NO3- | ||
| C. | Na+、K+、Cl-、NO3- | D. | Fe3+、K+、SO4 2-、Cl - |