题目内容
4.某中学的化学兴趣小组对SO2与漂白粉的反应进行实验探究,实验过程如下:取10克漂白粉固体,加入250mL水中,部分固体溶解溶液略有颜色,过滤后用洁净的玻璃棒沾取滤液到pH试纸上,发现pH试纸先变蓝(约为12)后褪色.回答下列问题:(1)工业制取漂白粉的化学方程式是2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉在空气中变质的原因Ca(ClO)2+CO2+H2O=CaCO3+2HClO(用化学反应方程式说明)
(2)pH试纸颜色的变化说明漂白粉溶液具有的性质是碱性和漂白性,ClO2和漂白粉一样也具有强氧化性,其消毒效率(以单位物质的量得电子的数目表示)是Cl2的2.5倍;
(3)将SO2持续通入漂白粉溶液中,发现澄清透明的溶液先变为黄绿色,随后溶液中产生大量白色沉淀且黄绿色褪去.回答下列问题:
①澄清透明溶液变为黄绿色的可能原因是:随溶液酸性的增强,漂白粉的有效成分和C1-发生反应.通过进一步实验确认了这种可能性,其实验方案是向漂白粉溶液中逐滴滴入硫酸,观察溶液颜色是否变为黄绿色;
②用离子方程式解释现象中黄绿色褪去的原因:Cl2+SO2+2H2O=4H++2Cl-+SO42-;
③SO2与漂白粉的有效成分在酸性条件下反应的离子方程式:2SO2+Ca2++2ClO-+2H2O=4H++2Cl-+CaSO4↓+SO42-.
分析 (1)氯气与石灰乳制备漂粉,漂白粉在空气中与二氧化碳、水反应生成HClO可变质;
(2)pH试纸先变蓝(约为12)后褪色,则溶液具有碱性、漂白性;利用电子转移计算消毒效率;
(3)SO2持续通入漂白粉溶液中,发现澄清透明的溶液先变为黄绿色,随后溶液中产生大量白色沉淀且黄绿色褪去,黄绿色气体为氯气,白色沉淀为硫酸钙,
①溶液酸性的增强,漂白粉的有效成分和C1-发生反应,则需要加酸;
②氯气与二氧化硫反应;
③SO2与漂白粉的有效成分在酸性条件下,发生氧化还原反应.
解答 解:(1)利用氢氧化钙和氯气发生反应生成次氯酸钙、氯化钙和水,反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉在空气中与二氧化碳、水反应生成HClO可变质,发生的反应为Ca(ClO)2+CO2+H2O=CaCO3+2HClO,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;Ca(ClO)2+CO2+H2O=CaCO3+2HClO;
(2)pH试纸先变蓝(约为12)后褪色,则溶液具有碱性、漂白性;ClO2和漂白粉一样也具有强氧化性,其消毒效率(以单位物质的量得电子的数目表示)是Cl2的$\frac{1mol×[4-(-1)]}{1mol×2×[0-(-1)]}$=2.5倍,故答案为:碱性和漂白性;2.5;
(3)SO2持续通入漂白粉溶液中,发现澄清透明的溶液先变为黄绿色,随后溶液中产生大量白色沉淀且黄绿色褪去,黄绿色气体为氯气,白色沉淀为硫酸钙,
①进一步实验确认了这种可能性,其实验方案是向漂白粉溶液中逐滴滴入硫酸,观察溶液颜色是否变为黄绿色,
故答案为:向漂白粉溶液中逐滴滴入硫酸,观察溶液颜色是否变为黄绿色;
②用离子方程式解释现象中黄绿色褪去的原因为Cl2+SO2+2H2O=4H++2Cl-+SO42-,故答案为:Cl2+SO2+2H2O=4H++2Cl-+SO42-;
③SO2与漂白粉的有效成分在酸性条件下反应的离子方程式为2SO2+Ca2++2ClO-+2H2O=4H++2Cl-+CaSO4↓+SO42-,故答案为:2SO2+Ca2++2ClO-+2H2O=4H++2Cl-+CaSO4↓+SO42-.
点评 本题考查二氧化硫和氯气的化学性质,为高频考点,综合考查元素化合物知识,把握物质的性质、实验设计及现象与结论的关系为解答的关键,侧重分析与实验能力的综合考查,题目难度不大.

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案①在水中氢、氧原子均以化学键相结合
②化学键是成键原子间的强烈吸引作用
③离子化合物通常条件下是固体
④难失去电子的原子,均易得电子形成阴离子
⑤根据电离方程式H2SO4═2H++SO42-,判断H2SO4中存在离子键
⑥单质分子中不存在化学键,化合物分子中才存在化学键
⑦H2分子和Cl2分子的反应过程是H2、Cl2分子里共价键发生断裂生成H、Cl原子,而后H、Cl原子形成离子键的过程.
| A. | ①②③正确 | B. | 都不正确 | ||
| C. | ⑥⑦正确,其它不正确 | D. | 仅③正确 |
| A. |  | B. |  | ||
| C. |  | D. |  |
| A. | 横线中的物质是Cu2S | B. | CuFeS2仅作还原剂 | ||
| C. | SO2是还原产物,不是氧化产物 | D. | FeS是氧化产物 |
| A. | 所有的非金属元素都分布在p区 | |
| B. | 元素周期表中ⅢB族到ⅡB族10个纵行的元素都是金属元素 | |
| C. | 在同一主族中,自上而下第一电离能逐渐减小 | |
| D. | 第ⅠA、ⅡA族元素的原子,其半径越大,电负性越小 |

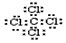 ,用一个离子方程式证明S(硫)元素和U元素的非金属性的强弱S2-+Cl2=S+2Cl-或H2S+Cl2=2H++2Cl-+S.
,用一个离子方程式证明S(硫)元素和U元素的非金属性的强弱S2-+Cl2=S+2Cl-或H2S+Cl2=2H++2Cl-+S.