题目内容
8.如图所示,已知A元素的最低化合价为-3价,它的最高价氧化物含氧56.21%,原子核内中子数比质子数多1,试回答:
(1)写出它们的元素符号:
AP,BS,CCl,DO,ESe.
(2)A、B、C、D的气态氢化物稳定性最差的是PH3.
(3)A、B、C的原子半径由小到大的顺序是Cl<S<P.
(4)A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是HClO4>H2SO4>H3PO4.
分析 A元素的最低化合价为-3价,则最高价为+5价,它的最高价氧化物为A2O5,含氧56.21%,设相对原子质量为x,则$\frac{80}{2x+80}$×100%=56.21%,解得x=31,故A为P元素,由元素在周期表中的位置可知,B为S,C为Cl,D为O,E为Se.
解答 解:(1)A元素的最低化合价为-3价,则最高价为+5价,它的最高价氧化物为A2O5,含氧56.21%,设相对原子质量为x,则$\frac{80}{2x+80}$×100%=56.21%,解得x=31,故A为P元素,由元素在周期表中的位置可知,B为S,C为Cl,D为O,E为Se,故答案为:P;S;Cl;O;Se;
(2)A、B、C、D中P元素非金属性最差,故气态氢化物稳定性最差的是:PH3,故答案为:PH3;
(3)同周期自左而右原子半径减小,故原子半径:Cl<S<P,故答案为:Cl<S<P;
(4)同周期自左而右非金属性增强,最高价含氧酸酸性增强,故酸性:HClO4>H2SO4>H3PO4,故答案为:HClO4>H2SO4>H3PO4.
点评 本题考查位置结构性质的关系及其应用,推断A是解答本题的关键,注意掌握元素周期律,难度不大.

练习册系列答案
相关题目
10.设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | NA个Fe(OH)3胶体粒子的质量为107g | |
| B. | 标准状况下,1L液态水中含有的H+数目为10-7NA | |
| C. | 14g分子式为CnH2n的链烃中含有的碳碳双键的数目为NA/n | |
| D. | 1 mol冰醋酸和l mo1乙醇经酯化反应可生成H2O分子数为NA |
16.表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素其原子结构示意图为 .
.
(2)表中能形成两性氢氧化物的元素其单质与⑨最高价氧化物的水化物反应的化学方程式2Al+2KOH+2H2O=2KAlO2+3H2↑.
(3)④元素与⑦元素形成化合物的电子式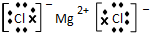 .
.
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4(填化学式).
(5)在⑨与④的单质中,化学性质较活泼的是K,①、②的气态氢化物中,比较稳定的是NH3(填化学式).
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)表中能形成两性氢氧化物的元素其单质与⑨最高价氧化物的水化物反应的化学方程式2Al+2KOH+2H2O=2KAlO2+3H2↑.
(3)④元素与⑦元素形成化合物的电子式
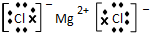 .
.(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4(填化学式).
(5)在⑨与④的单质中,化学性质较活泼的是K,①、②的气态氢化物中,比较稳定的是NH3(填化学式).
13.一定温度下,在固定体积的密闭容器中发生下列反应:2HI(g)=H2(g)+I2(g)若c(HI) 由0.1mol/L
降到0.07mol/L时,需要15s,那么c(HI)由0.07mol/L降到0.05mol/L时,所需反应时间为( )
降到0.07mol/L时,需要15s,那么c(HI)由0.07mol/L降到0.05mol/L时,所需反应时间为( )
| A. | 等于5s | B. | 等于10s | C. | 大于10s | D. | 小于10s |
20.卤素是最活泼的一族非金属,下列关于卤族元素的说法正确的是( )
| A. | 卤素元素原子最外层电子数都是7 | B. | 从氟到碘,卤素原子半径依次减小 | ||
| C. | 卤素元素单质均为气态 | D. | 从氟到碘,非金属性逐渐增强 |
17.检验某未知溶液中是否含SO42-的下列操作中,合理的是( )
| A. | 先加硝酸酸化,再加氯化钡溶液 | B. | 先加硝酸酸化,再加硝酸钡溶液 | ||
| C. | 先加盐酸酸化,再加氯化钡溶液 | D. | 先加盐酸酸化,再加硝酸铜溶液 |
18.在生活、生产及化学研究中,人们经常需要根据不同原子、分子或离子的某些特征反应对物质进行检验,以确定物质的组成.下列有关物质检验的说法正确的是( )
| A. | MnO2、CuO、Fe三种物质的粉末都是黑色的,用稀盐酸不能将它们区别开 | |
| B. | (NH4)2SO4、K2SO4、NH4C1三种物质不能用一种试剂通过化学反应区别开 | |
| C. | 可以用BaCl2溶液和稀硝酸检验Na2SO3 是否变质 | |
| D. | 用湿润的KI淀粉试纸可以检验氯化氢气体中是否含有氯气 |