题目内容
10.下列有关实验操作的叙述中正确的是( )| A. |  利用甘油密度大于乙醇且更易溶于水,进行甘油与乙醇的混合物分离 | |
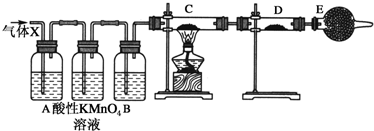
| B. | 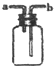 进行H2,NH3,CO2,Cl2,HCl,NO2等气体收集,也能用于NO气体收集 | |
| C. |  当X选用苯时可进行NH3和HCl的吸收,并防止倒吸 | |
| D. | 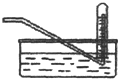 常用于实验室收集氧气、氢气等 |
分析 A.甘油与乙醇互溶;
B.与氧气反应的气体不能使用排空气法收集,a进气收集密度比空气小的气体,b进气收集密度比空气大的气体;
C.苯的密度比水小,不能隔绝气体与水;
D.氧气、氢气不溶于水,不与水反应.
解答 解:A.甘油与乙醇不分层,不能利用与中分液装置分离,故A错误;
B.与氧气反应的气体不能使用排空气法收集,a进气收集密度比空气小的气体,b进气收集密度比空气大的气体,则装置可进行H2,NH3,CO2,Cl,HCl,NO2等气体收集,但不能用于NO气体收集,故B错误;
C.苯的密度比水小,不能隔绝气体与水,则X为苯时不能防止倒吸,应选四氯化碳,故C错误;
D.氧气、氢气不溶于水,不与水反应,可用排水法收集,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、气体的收集及防倒吸装置等,把握物质的性质及反应原理为解答的关键,侧重分析与应用能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
3.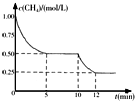 密闭容器中有反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)变化如右图所示.下列判断正确的是( )
密闭容器中有反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)变化如右图所示.下列判断正确的是( )
 密闭容器中有反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)变化如右图所示.下列判断正确的是( )
密闭容器中有反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)变化如右图所示.下列判断正确的是( )| A. | 0~5 min内,v(H2)=0.1 mol/(L•min) | |
| B. | 10 min时改变的外界条件可能是升高温度 | |
| C. | 恒温下,缩小容器体积,平衡后c(H2)减小 | |
| D. | 12 min时反应达平衡的本质原因是气体总质量不再变化 |
1.下列不属于有机物的原子成键特点的是( )
| A. | 碳原子易失去最外层的电子形成离子 | |
| B. | 碳原子最外层电子易于其他原子的外层电子形成共同电子对 | |
| C. | 组成有机物的碳原子可以形成单键、双键和三键等多种成键形式 | |
| D. | 组成有机物的氧原子、氮原子、卤素原子分别形成2个、3个、1个共价键 |
5.乙醛能与银氨溶液反应析出银,如果条件控制适当,析出的银会均匀分布在试管上,形成光亮的银镜,这个反应叫银镜反应.银镜的光亮程度与反应条件有关,某课外活动小组同学在课外活动中对乙醛的银镜反应进行了探究.
Ⅰ.探究银镜反应的最佳实验条件的部分实验数据如下表:
请回答下列问题:
(1)若只进行实验1和实验3,其探究目的是比较乙醛用量不同,生成银镜的时间(速度或质量均可).
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间范围是在6.5~9min之间.
(3)进一步实验还可探索银氨溶液的用量不同或pH不同对出现银镜快慢的影响.
Ⅱ.探究对废液的回收处理:银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环
境,且造成银资源的浪费.通过查找资料,已知从银氨溶液中提取银的一种实验流程如下:
$→_{①}^{(NH_{4})_{2}S}$$→_{②}^{过滤、洗涤}$$→_{③}^{烘干}$Ag2S$→_{④}^{铁粉还原}$银粉
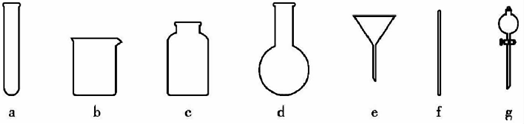
(4)操作④的方法是把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉,反应的化学方程式为Ag2S+Fe+2HCl$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+FeCl2+H2S↑.过滤需要用到的玻璃仪器有bef(填编号).要得到纯净的Ag2S沉淀,需要洗涤沉淀,实验室过滤器中洗涤沉淀的操作是:沿着玻璃棒向过滤器注入蒸馏水浸没沉淀,水自然流下,重复2~3次.
(5)根据电化原理也可Ag2S转变为Ag,方法是:在铝质容器中加入食盐溶液,再将表面生成Ag2S的银器浸入该溶液中,一段时间后发现黑色会褪去.
①该装置中银器为正极.
②该装置总反应的化学方程式为2Al+3Ag2 S+3H2O=2Al(OH)3+6Ag+3H2S↑.
Ⅰ.探究银镜反应的最佳实验条件的部分实验数据如下表:
| 实验序号 | 银氨溶液 | 乙醛的量/滴 | 水浴温度/℃ | 反应混合液的pH | 出现银镜时间 |
| 1 | 1 | 3 | 65 | 11 | 5 |
| 2 | 1 | 3 | 45 | 11 | 6.5 |
| 3 | 1 | 5 | 65 | 11 | 4 |
| 4 | 1 | 3 | 30 | 11 | 9 |
| 5 | 1 | 3 | 50 | 11 | 6 |
| 6 | 1 | 5 | 80 | 11 | 3 |
(1)若只进行实验1和实验3,其探究目的是比较乙醛用量不同,生成银镜的时间(速度或质量均可).
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间范围是在6.5~9min之间.
(3)进一步实验还可探索银氨溶液的用量不同或pH不同对出现银镜快慢的影响.
Ⅱ.探究对废液的回收处理:银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环
境,且造成银资源的浪费.通过查找资料,已知从银氨溶液中提取银的一种实验流程如下:
$→_{①}^{(NH_{4})_{2}S}$$→_{②}^{过滤、洗涤}$$→_{③}^{烘干}$Ag2S$→_{④}^{铁粉还原}$银粉
(4)操作④的方法是把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉,反应的化学方程式为Ag2S+Fe+2HCl$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+FeCl2+H2S↑.过滤需要用到的玻璃仪器有bef(填编号).要得到纯净的Ag2S沉淀,需要洗涤沉淀,实验室过滤器中洗涤沉淀的操作是:沿着玻璃棒向过滤器注入蒸馏水浸没沉淀,水自然流下,重复2~3次.

(5)根据电化原理也可Ag2S转变为Ag,方法是:在铝质容器中加入食盐溶液,再将表面生成Ag2S的银器浸入该溶液中,一段时间后发现黑色会褪去.
①该装置中银器为正极.
②该装置总反应的化学方程式为2Al+3Ag2 S+3H2O=2Al(OH)3+6Ag+3H2S↑.
2.用Na2CO3固体配制一定物质的量浓度的Na2CO3溶液时,不需要使用的玻璃仪器是( )
| A. | 玻璃棒 | B. | 分液漏斗 | C. | 容量瓶 | D. | 胶头滴管 |
19.实验中需要1mol/L的CuSO4溶液480mL,配制溶液时需要称取( )
| A. | 125.0克CuSO4•5H2O 晶体 | B. | 76.8克无水CuSO4 固体 | ||
| C. | 120.0克CuSO4•5H2O 晶体 | D. | 40.0克无水CuSO4固体 |
20.将20g铁粉放入一定量的稀硝酸中,充分反应后,放出2.24L(标准状况)NO气体,铁粉有剩余,则剩余的铁粉的质量是( )
| A. | 14.4 g | B. | 11.6 g | C. | 8.8 g | D. | 3.2 g |