题目内容
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题.
(1)写出CO2与H2反应生成CH4和H2O的热化学方程式.
已知:①CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41kJ?mol-1
②C(s)+2H2(g)?CH4(g)△H=-73kJ?mol-1
③2CO(g)?C(s)+CO2(g)△H=-171kJ?mol-1
(2)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)
CH3OCH3(g)+3H2O(g)
已知一定条件下,该反应中CO2的平衡转化率随温度、投料比[
]的变化曲线如图1:
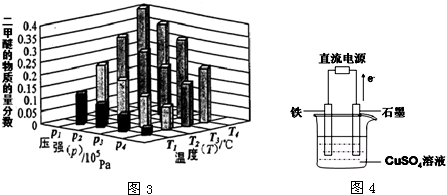
①在其他条件不变时,请在上图2中画出平衡时CH3OCH3的体积分数随投料比[
]变化的曲线图.
②某温度下,将2.0mol CO2(g)和6.0mol(g)充入容积为2L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如图3所示,关于温度和压强的关系判断正确的是 ;
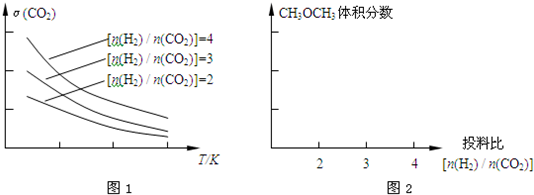
A.P3>P2,T3>T2 B.P1>P3,T1>T3 C.P2>P4,T4>T2 D.P1>P4,T2>T3
③在恒容密闭容器里按体积比为1:3充入二氧化碳和氢 气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是 ;
A.正反应速率先增大后减小 B.逆反应速率先增大后减小
C.化学平衡常数K值增大 D.反应物的体积百分含量增大
E.混合气体的密度减小 F.氢气的转化率减小
(3)最近科学家再次提出“绿色化学”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇.甲醇可制作燃料电池,写出以稀硫酸为电解质甲醇燃料电池负极反应式 .以此燃料电池作为外接电源按如图4所示电解硫酸铜溶液,如果起始时盛有1000mL pH=5的硫酸铜溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1,此时可观察到的现象是 ;若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入 (填物质名称),其质量约为 g.
(1)写出CO2与H2反应生成CH4和H2O的热化学方程式.
已知:①CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41kJ?mol-1
②C(s)+2H2(g)?CH4(g)△H=-73kJ?mol-1
③2CO(g)?C(s)+CO2(g)△H=-171kJ?mol-1
(2)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)
| 催化剂 |
已知一定条件下,该反应中CO2的平衡转化率随温度、投料比[
| n(H2) |
| n(CO2) |
①在其他条件不变时,请在上图2中画出平衡时CH3OCH3的体积分数随投料比[
| n(H2) |
| n(CO2) |
②某温度下,将2.0mol CO2(g)和6.0mol(g)充入容积为2L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如图3所示,关于温度和压强的关系判断正确的是

A.P3>P2,T3>T2 B.P1>P3,T1>T3 C.P2>P4,T4>T2 D.P1>P4,T2>T3
③在恒容密闭容器里按体积比为1:3充入二氧化碳和氢 气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是
A.正反应速率先增大后减小 B.逆反应速率先增大后减小
C.化学平衡常数K值增大 D.反应物的体积百分含量增大
E.混合气体的密度减小 F.氢气的转化率减小
(3)最近科学家再次提出“绿色化学”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇.甲醇可制作燃料电池,写出以稀硫酸为电解质甲醇燃料电池负极反应式

考点:用盖斯定律进行有关反应热的计算,化学电源新型电池,化学平衡的影响因素
专题:化学反应中的能量变化,化学平衡专题,电化学专题
分析:(1)根据盖斯定律来计算热化学方程式的焓变;
(2)①根据化学方程式的系数进行回答;
②根据温度和压强对化学平衡的影响:升高温度,平衡向着吸热方向进行,增大压强,化学平衡向着气体系数和减小的方向进行来回答;
③当正逆反应速率不相等时,化学平衡会向着正方向或是逆方向进行;
(3)在燃料点池中,负极上发生失电子的氧化反应,根据电解硫酸铜溶液的反应特征分析判断恢复溶液浓度.
(2)①根据化学方程式的系数进行回答;
②根据温度和压强对化学平衡的影响:升高温度,平衡向着吸热方向进行,增大压强,化学平衡向着气体系数和减小的方向进行来回答;
③当正逆反应速率不相等时,化学平衡会向着正方向或是逆方向进行;
(3)在燃料点池中,负极上发生失电子的氧化反应,根据电解硫酸铜溶液的反应特征分析判断恢复溶液浓度.
解答:
解:(1)CO2与H2反应生成CH4和H2O的化学方程式为:CO2(g)+4H2(g) CH4(g)+2H2O(g),
CH4(g)+2H2O(g),
已知:①CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41kJ?mol-1
②C(s)+2H2(g)?CH4(g)△H=-73kJ?mol-1
③2CO(g)?C(s)+CO2(g)△H=-171kJ?mol-1
根据盖斯定律,反应CO2(g)+4H2(g) CH4(g)+2H2O(g)可以是②+③-①×2得到,
CH4(g)+2H2O(g)可以是②+③-①×2得到,
所以反应的△H=(-73kJ?mol-1+(-171kJ?mol-1)-2×(-41kJ?mol-1)=-162kJ?mol-1,
故答案为:CO2(g)+4H2(g) CH4(g)+2H2O(g),△H=-162kJ?mol-1;
CH4(g)+2H2O(g),△H=-162kJ?mol-1;
(2)①CH3OCH3的体积分数随投料比[n(H2)/n(CO2)]的增大而增大,根据反应知道当体积比是3的时候,甲醚的体积分数最大,如下图所示:
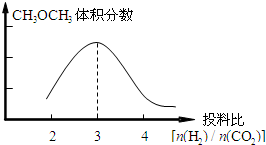 ,故答案为:
,故答案为: ;
;
②根据图三可以看出,对于反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H<0,压强越大,甲醇的物质的量分数则越大,温度越高,甲醇的物质的量分数越小,所以P1>P3、T1>T3,P1>P4、T2>T3,故答案为:BD;
③化学平衡的标志是正逆反应速率相等,当逆反应速率大于正反应速率时,说明反应是逆向进行的,故答案为:B;
(3)在燃料电池中,负极上是燃料甲醚发生失电子的氧化反应,电极反应式为:CH3OH+H2O-6e-=CO2+6H+,惰性电极电解硫酸铜溶液生成铜、氧气、硫酸,恢复原溶液浓度需要加入析出的物质,即加入氧化铜可以恢复,阳极上的反应:4OH--4e-═O2↑+2H2O,当溶液pH=1时,氢离子浓度是0.1mol/L,所以减少的氢氧根离子是0.1mol,产生氧气物质的量是0.025mol,含有氧元素的物质的量是0.05mol,需要加入氧化铜的物质的量是0.05mol,质量是0.05mol×80g/mol=4g,
故答案为:CH3OH+H2O-6e-=CO2+6H+;氧化铜;4g.
 CH4(g)+2H2O(g),
CH4(g)+2H2O(g),已知:①CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41kJ?mol-1
②C(s)+2H2(g)?CH4(g)△H=-73kJ?mol-1
③2CO(g)?C(s)+CO2(g)△H=-171kJ?mol-1
根据盖斯定律,反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g)可以是②+③-①×2得到,
CH4(g)+2H2O(g)可以是②+③-①×2得到,所以反应的△H=(-73kJ?mol-1+(-171kJ?mol-1)-2×(-41kJ?mol-1)=-162kJ?mol-1,
故答案为:CO2(g)+4H2(g)
 CH4(g)+2H2O(g),△H=-162kJ?mol-1;
CH4(g)+2H2O(g),△H=-162kJ?mol-1;(2)①CH3OCH3的体积分数随投料比[n(H2)/n(CO2)]的增大而增大,根据反应知道当体积比是3的时候,甲醚的体积分数最大,如下图所示:
 ,故答案为:
,故答案为: ;
;②根据图三可以看出,对于反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H<0,压强越大,甲醇的物质的量分数则越大,温度越高,甲醇的物质的量分数越小,所以P1>P3、T1>T3,P1>P4、T2>T3,故答案为:BD;
③化学平衡的标志是正逆反应速率相等,当逆反应速率大于正反应速率时,说明反应是逆向进行的,故答案为:B;
(3)在燃料电池中,负极上是燃料甲醚发生失电子的氧化反应,电极反应式为:CH3OH+H2O-6e-=CO2+6H+,惰性电极电解硫酸铜溶液生成铜、氧气、硫酸,恢复原溶液浓度需要加入析出的物质,即加入氧化铜可以恢复,阳极上的反应:4OH--4e-═O2↑+2H2O,当溶液pH=1时,氢离子浓度是0.1mol/L,所以减少的氢氧根离子是0.1mol,产生氧气物质的量是0.025mol,含有氧元素的物质的量是0.05mol,需要加入氧化铜的物质的量是0.05mol,质量是0.05mol×80g/mol=4g,
故答案为:CH3OH+H2O-6e-=CO2+6H+;氧化铜;4g.
点评:本题是一道关于热化学、电化学、化学反应速率和平衡知识的综合考查题,要求学生具有分析和解决问题的能力,综合性强,难度大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
X、Y均为短周期主族元素,X原子的最外层有2个电子,Y原子的最外层有6个电子,这两种元素形成的常见化合物的化学式为( )
| A、XY |
| B、XY2 |
| C、X2Y |
| D、X2Y3 |
同温同压下,相同质量的下列气体所含分子数最多的是( )
| A、H2 |
| B、CH4 |
| C、NO |
| D、CO2 |
 ,则其单体的结构简式为
,则其单体的结构简式为

 看,分子中含有碳碳双键,由此推测,苯能使酸性高锰酸钾溶液褪色且苯的6个碳原子之间的键有两种.
看,分子中含有碳碳双键,由此推测,苯能使酸性高锰酸钾溶液褪色且苯的6个碳原子之间的键有两种.
 Ⅰ、碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:W(s)+I2(g)?WI2(g).
Ⅰ、碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:W(s)+I2(g)?WI2(g).