题目内容
下列溶液中有关物质的量浓度关系错误的是( )
| A、pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(H+)+c(M+)═c(OH-)+c(A-) |
| B、pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa) |
| C、物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)═2c(H+)+c(CH3COOH) |
| D、0.1mol?L-1的NaHA溶液,其pH=4:c(Na+)>c(H+)>c(H2A)>c(A2-) |
考点:离子浓度大小的比较
专题:
分析:A、根据电荷守恒分析解答;
B、相同浓度的三种溶液CH3COONa、NaOH和Na2CO3pH的大小分别为NaOH、Na2CO3和CH3COONa,所以pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa);
C、物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合,溶液显酸性,电荷守恒为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),物料守恒为c(CH3COO-)+c(CH3COOH)=0.1mol/L=2c(Na+),以此分析;
D、0.1mol?L-1的NaHA溶液,其pH=4,电离大于水解程度.
B、相同浓度的三种溶液CH3COONa、NaOH和Na2CO3pH的大小分别为NaOH、Na2CO3和CH3COONa,所以pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa);
C、物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合,溶液显酸性,电荷守恒为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),物料守恒为c(CH3COO-)+c(CH3COOH)=0.1mol/L=2c(Na+),以此分析;
D、0.1mol?L-1的NaHA溶液,其pH=4,电离大于水解程度.
解答:
解:A、根据电荷守恒,可知c(H+)+c(M+)═c(OH-)+c(A-),故A正确;
B、相同浓度的三种溶液CH3COONa、NaOH和Na2CO3pH的大小分别为NaOH、Na2CO3和CH3COONa,所以pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa),故B正确;
C、物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合,溶液显酸性,电荷守恒为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),物料守恒为c(CH3COO-)+c(CH3COOH)=0.1mol/L=2c(Na+),由上述两个式子可得c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-),故C正确;
D、0.1mol?L-1的NaHA溶液,其pH=4,电离大于水解程度,所以离子浓度大小为:c(Na+)>c(H+)>c(A2-)>c(H2A),故D错误;
故选D.
B、相同浓度的三种溶液CH3COONa、NaOH和Na2CO3pH的大小分别为NaOH、Na2CO3和CH3COONa,所以pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa),故B正确;
C、物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合,溶液显酸性,电荷守恒为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),物料守恒为c(CH3COO-)+c(CH3COOH)=0.1mol/L=2c(Na+),由上述两个式子可得c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-),故C正确;
D、0.1mol?L-1的NaHA溶液,其pH=4,电离大于水解程度,所以离子浓度大小为:c(Na+)>c(H+)>c(A2-)>c(H2A),故D错误;
故选D.
点评:本题考查离子浓度的大小结合盐的水解知识,学生在解题中要注意守恒知识的应用,比较容易.

练习册系列答案
相关题目
下列物质能与氢氧化钠溶液反应,但不与盐酸反应的是( )
| A、氢氧化铝 | B、氧化铝 |
| C、二氧化硅 | D、铝 |
在2A(g)+B(g)=3C(g)+4D(g)中,表示该反应速率最快的是( )
| A、v(A)=0.5mol?L-1.mim-1 |
| B、v(B)=0.3mol?L-1.mim-1 |
| C、v(C)=0.8mol?L-1.mim-1 |
| D、v(D)=1.0mol?L-1.mim-1 |
铵盐受热易分解,但硝酸铵在不同条件下分解所得产物不同.下列各组物质中可能是硝酸铵分解产物的是( )
| A、O2+HNO3+H2O |
| B、N2+NH3+H2O |
| C、NH3+HNO3 |
| D、NH3+NO+H2 |
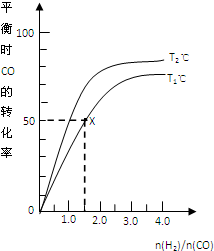 在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g)+2H2(g)CH3OH(g)△H<0有关信息如图所示,下列说法正确的是( )
在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g)+2H2(g)CH3OH(g)△H<0有关信息如图所示,下列说法正确的是( )| A、T1<T2 | ||
| B、T1℃时该反应的平衡常数为4.0 | ||
C、同一温度下,
| ||
D、相同条件下
|
下列排序正确的是( )
| A、酸性:H2CO3<H2SiO3<CH3COOH |
| B、碱性:Ba(OH)2<Ca(OH)2<KOH |
| C、熔点:MgBr2<CCl4<SiO2 |
| D、沸点:PH3<NH3<H2O |
中美两国11月11日在北京APEC会议上达成温室气体减排协议,并发表联合声明.中国将力争实现温室气体排放量到2030年左右达到峰值.美国则承诺2025年温室气体排放量较2005年下降近四分之一.下列有关CO2排放的说法中正确的是( )
| A、开发太阳能、氢能等新型能源有利于减少二氧化碳的排放量 |
| B、煤的气化技术是减少二氧化碳排放的重要措施 |
| C、减少二氧化碳的排放有利于减少酸雨对环境的污染 |
| D、“不允许向大气中排放二氧化碳”是《京都议定书》的重要精神 |