题目内容
2.某陨石中含有镁元素的一种同位素${\;}_{12}^{28}$Mg,下列对该同位素描述正确的是( )| A. | 质量数为12 | B. | 核电荷数为12 | ||
| C. | 电子数为28 | D. | 中子数与质子数之差为16 |
分析 根据原子符号中左上角数字为质量数,左下角数字为质子数,中子数=质量数-质子数,核外电子数=质子数=核电荷数来解答.
解答 解:同位素${\;}_{12}^{28}$Mg的质子数为12,质量数为28,核外电子数=质子数=核电荷数=12,中子数=28-12=16,中子数与质子数之差为4,故选B.
点评 本题主要考查了原子的组成以及各个量之间的关系,难度不大,属于基础题.

练习册系列答案
相关题目
12.某化学课外小组的同学通过实验探究温度和浓度对反应速率的影响.
实验原理及方案:在酸性溶液中,碘酸钾( KIO3)和亚硫酸钠可发生反应生成碘,反应原理是2IO3-+5SO32-+2H+=I2+5SO42-+H2O,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率.
(1)V1=40mL,V2=10mL.
(2)从你的理解看最先出现蓝色的一组实验是③ (填序号)
实验原理及方案:在酸性溶液中,碘酸钾( KIO3)和亚硫酸钠可发生反应生成碘,反应原理是2IO3-+5SO32-+2H+=I2+5SO42-+H2O,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率.
| 实验 序号 | 0.01mol/L KIO3酸性溶液 (含淀粉)的体积/mL | 0.01mol/L Na2SO3溶 液的体积/mL | 水的体 积/mL | 实验温 度/℃ | 出现蓝色 的时间/s |
| ① | 5 | 5 | V1 | 0 | |
| ② | 5 | 5 | 40 | 25 | |
| ③ | 5 | V2 | 35 | 25 |
(2)从你的理解看最先出现蓝色的一组实验是③ (填序号)
13.下列与有机物的结构、性质相关的叙述错误的是( )
| A. | 碳碳双键不可旋转所以烯烃一定有顺反异构 | |
| B. | 由乙烯、乙炔的结构特点可推知CH3-CH=C(CH3)-C≡C-CH3分子中所有的碳原子共面 | |
| C. | 甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同 | |
| D. | 苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有乙烯分子中类似的碳碳双键 |
10.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 丙烯分子有7个σ键,1个π键 | |
| B. | 由2H和18O所组成的水11g,其中所含的中子数为4NA | |
| C. | 0.1mol SiO2晶体中所含有的硅氧键数目为0.2NA | |
| D. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3mol I2转移的电子数为5NA个 |
7.下列现象与氢键有关的是( )
①NH3的熔、沸点比VA族其他元素氢化物的高
②乙醇、乙酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④水分子高温下也很稳定.
①NH3的熔、沸点比VA族其他元素氢化物的高
②乙醇、乙酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④水分子高温下也很稳定.
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ②③④ |
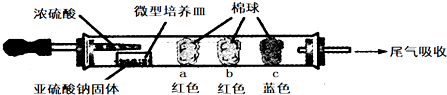
14.硬质玻璃管进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表.
请填写表中的空白:

请填写表中的空白:
| 棉球 | 棉球上滴加的试剂 | 实验现象 | 解释和结论 |
| a | 品红试液 | 棉球变白,微热后又恢复红色 | |
| b | 含酚酞的NaOH溶液 | 棉球变为白色 | 离子方程式: 2OHˉ+SO2=SO32ˉ+H2O 或OHˉ+SO2=HSO3ˉ |
| c | 含淀粉的碘水 | 棉球变为白色 | 结论:该气体具有还原 性 |
12. 氮、硫、氯、钠、铝、铁及其化合物是研究基本概念和基本理论的重要载体.
氮、硫、氯、钠、铝、铁及其化合物是研究基本概念和基本理论的重要载体.
(1)角“>”“<”或“=”填空:
(2)在N、S、Cl的含氧酸的阴离子中,空间构型呈三角锥形的有SO32-、ClO3-(填离子符号);在NH3、H2S中,键角较大的是NH3,理由是氨气电子中含有1对孤对电子,H2S分子中含有2对孤对电子,孤电子对越多,对成键电子对的排斥越大,键角越小.
(3)(SCN)2分子中每个原子最外层都达到稳定结构,(SCN)2分子中σ键和π键数目之比为5:4.
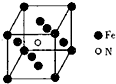
(4)某种磁性氮化铁晶胞如图所示.
①该晶体的化学式为Fe4N.
②已知该晶胞体积为V cm3,该晶胞的密度为$\frac{238}{V{N}_{A}}$g•cm-3(NA表示阿伏加德罗常数的值).
 氮、硫、氯、钠、铝、铁及其化合物是研究基本概念和基本理论的重要载体.
氮、硫、氯、钠、铝、铁及其化合物是研究基本概念和基本理论的重要载体.(1)角“>”“<”或“=”填空:
| 性质 | 第一电离能 | 熔点 | 半径 | 键能 |
| 对象 | S<Cl | Na<Al | N3->Al3+ | N=N<N≡N |
(3)(SCN)2分子中每个原子最外层都达到稳定结构,(SCN)2分子中σ键和π键数目之比为5:4.
(4)某种磁性氮化铁晶胞如图所示.
①该晶体的化学式为Fe4N.
②已知该晶胞体积为V cm3,该晶胞的密度为$\frac{238}{V{N}_{A}}$g•cm-3(NA表示阿伏加德罗常数的值).