题目内容
17.针对如图装置的说法中,正确是( )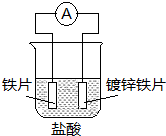
| A. | 溶液中pH值明显下降 | B. | 阴极的电极反应式:Fe-2e→Fe2+ | ||
| C. | 铁片为正极,镀锌铁片为负极 | D. | 电子由锌经溶液流向铁 |
分析 锌比铁活泼,锌为负极,发生氧化反应,电极方程式为Zn-2e-=Zn2+,铁为正极,发生还原反应,电极方程式为2H++2e-=H2↑,以此解答.
解答 解:A.正极发生2H++2e-=H2↑,溶液氢离子浓度降低,pH增大,故A错误;
B.为原电池,电极为正极、负极,不存在阴极、阳极,故B错误;
C.锌比铁活泼,锌为负极,铁片为正极,故C正确;
D.电子由负极经导线流向正极,故D错误.
故选C.
点评 本题考查了原电池原理,明确原电池和电解池的判断方法,再结合金属失电子的难易程度确定正负极,难点是电极反应式的书写,要结合电解质溶液酸碱性书写,题目难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
9.下列物质的变化,不能通过一步化学反应完成的是( )
| A. | CO2→H2CO3 | B. | Al(OH)3→Al2O3 | C. | Na2O2→Na2CO3 | D. | SiO2→H2SiO3 |
9.如图所示铜锌原电池工作时,下列叙述正确的是( )


| A. | 正极反应为:Zn-2e-═Zn2+ | |
| B. | 电池反应为:Zn+Cu2+═Zn2++Cu | |
| C. | 在外电路中,电子从铜电极流向锌电极 | |
| D. | 盐桥中的K+移向ZnSO4溶液 |
6.下列对应操作正确且能达到实验目的是( )
| A. |  用图装置验证化学能转化为电能 | B. |  用图装置量取15.00mL KMnO4溶液 | ||
| C. | 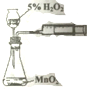 用图装置测定该化学反应速率 | D. | 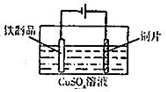 用图装置在铁制品表面镀铜 |
7.关于物质的量浓度溶液的配置说法正确的是( )
| A. | 容量瓶在使用之前要检漏 | |
| B. | 容量瓶上有温度,浓度,标线三个标识 | |
| C. | 定容时,因不慎使液面高于容量瓶的刻度线,可用滴管将多余液体吸出 | |
| D. | 配置好的溶液储存在容量瓶中,并贴上标签 |