题目内容
17.已知25℃时,CaCO3饱和溶液中c(Ca2+)=5.3×10-5mol•L-1,MgCO3的饱和溶液中c(Mg2+)=2.6×10-3mol•L-1.若在5mL浓度均为0.01mol•L-1的CaCl2和MgCl2的混合溶液中加入5mL0.012mol•L-1的Na2CO3溶液,充分反应后过滤得到滤液M和沉淀N(不考虑溶液的体积变化),下列说法不正确的是( )| A. | 25℃时,Ksp(CaCO3)=2.8×10-9 | |
| B. | 加入Na2CO3溶液的过程中,先生成CaCO3沉淀 | |
| C. | 滤液M中c(Cl-)>c(Na+)>c(Mg2+)>c(CO32-)>c(OH-) | |
| D. | 滤液M中$\frac{c(C{a}^{2+})}{c(M{g}^{2+})}$=$\frac{{K}_{sp}(CaC{O}_{3})}{{K}_{sp}(MgC{O}_{3})}$ |
分析 A.根据Ksp=c(Ca2+)×c(CO32-)计算;
B.Ksp越小,越易生成沉淀;
C.计算混合后各离子浓度,可比较大小;
D.结合C的计算,溶液中没有生成碳酸镁沉淀.
解答 解:A.CaCO3饱和溶液中c(Ca2+)=5.3×10-5mol•L-1,则c(CO32-)=5.3×10-5mol•L-1,Ksp=c(Ca2+)×c(CO32-)=5.3×10-5×5.3×10-5=2.8×10-9,故A正确;
B.Ksp(CaCO3)=2.8×10-9,Ksp(MgCO3)=2.6×10-3×2.6×10-3=6.76×10-6,Ksp(CaCO3)较小,先生成CaCO3沉淀,故B正确;
C.在5mL浓度均为0.01mol•L-1的CaCl2和MgCl2的混合溶液中加入5mL0.012mol•L-1的Na2CO3溶液,如先不考虑离子之间的反应,混合后c(Ca2+)=0.005mol•L-1,(Mg2+)=0.005mol•L-1,c(Cl-)=0.02mol•L-1,c(CO32-)=0.006mol•L-1,c(Na+)=0.012mol•L-1,c(Ca2+)×c(CO32-)=3×10-5>2.8×10-9,则先生成碳酸钙沉淀,后剩余c(CO32-)=0.001mol•L-1,此时(Mg2+)=0.005mol•L-1,则c(Cl-)>c(Na+)>c(Mg2+)>c(CO32-)>c(OH-),故C正确;
D.由C可知,混合后c(Ca2+)=0.005mol•L-1,(Mg2+)=0.005mol•L-1,c(CO32-)=0.006mol•L-1,c(Ca2+)×c(CO32-)=3×10-5,c(Mg2+)×c(CO32-)=5×10-6<6.76×10-6,没有碳酸镁沉淀生成,溶液中不存在MgCO3(s)+Ca2+(aq)?CaCO3(s)+Mg2+(aq),故D错误.
故选D.
点评 本题考查了难溶电解质的溶解平衡及其应用,题目难度中等,注意结合溶度积常数来分析解答,试题培养了学生的分析能力及灵活应用基础知识的能力.

| A. | Fe2O3是氧化剂 | |
| B. | Na2FeO4既是氧化产物又是还原产物 | |
| C. | 生成1mol Na2FeO4时,有3mol电子转移 | |
| D. | Na2FeO4能杀菌消毒是利用Na2FeO4中+6价铁的强还原性被还原为Fe3+,净水是利用Fe3+在水中产生Fe(OH)3胶体从而吸附水中的悬浮颗粒 |
| A. | 单质硅是将太阳能转化为电能的常用材料 | |
| B. | CaO能与SO2反应,可作工业废气的脱硫剂 | |
| C. | 明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 | |
| D. | 镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 |
| A | B | C | |
| 浓度1 | 0.05mol•L-1 | a mol•L-1 | 0.05mol•L-1 |
| 浓度2 | 0.078mol•L-1 | 0.078mol•L-1 | 0.022mol•L-1 |
| 浓度3 | 0.06mol•L-1 | 0.06mol•L-1 | 0.04mol•L-1 |
| 浓度4 | 0.07mol•L-1 | 0.07mol•L-1 | 0.098mol•L-1 |
| A. | 由[浓度3]与[浓度1]的比较,可判断平衡移动的原因是增大了体系的压强 | |
| B. | 由[浓度2]与[浓度1]的比较,可判断正反应是放热反应 | |
| C. | [浓度1]中a=0.05 | |
| D. | 该组某学生在实验①过程中,测得各物质在某一时刻的浓度为[浓度4].与[浓度1]比较,可发现该同学在测定[浓度4]这组数据时出现了很大的误差 |
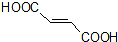 的合成路线如下:
的合成路线如下: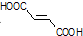
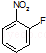 中含有的官能团名称为硝基,氟原子.
中含有的官能团名称为硝基,氟原子.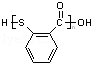 .
.
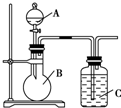 某同学设计如图装置,研究非金属元素性质变化规律.
某同学设计如图装置,研究非金属元素性质变化规律.