题目内容
11.3.1g Na2X含有Na+ 0.1mol,则Na2X的摩尔质量为62g/mol,X的相对原子质量为16.分析 由钠离子计算Na2X的物质的量,再根据M=$\frac{m}{n}$计算Na2X的摩尔质量,进而计算X的相对原子质量.
解答 解:3.1g Na2X中含有0.1mol Na+,Na2X的物质的量为:$\frac{0.1mol}{2}$=0.05mol,Na2X的摩尔质量为:$\frac{3.1g}{0.05mol}$=62g/mol,X的相对原子质量为:62-23×2=16,
故答案为:62g/mol;16.
点评 本题考查物质的量有关计算,题目难度不大,注意掌握以物质的量为中心的有关计算,试题侧重基础知识的考查,培养了学生的化学计算能力.

练习册系列答案
相关题目
18.下列涉及的有机物及有机反应类型正确的是( )
| A. | 乙烯分子与苯分子均含碳碳双键,都能发生加成反应 | |
| B. | 除去甲烷气体中的乙烯可将混合气体通过盛有足量酸性高锰酸钾溶液的洗气瓶 | |
| C. | 实验室可用溴水鉴别苯、乙醇和环己烯 | |
| D. | 乙酸和乙醇在浓硫酸作用下可以反应,该反应属于加成反应 |
19.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 22.4 LCl2分别与铁和铜反应时,失电子数目均为NA | |
| B. | 7.8g Na2O2加入过量水中,反应转移的电子数为0.2 NA | |
| C. | 常温常压下,14 g 氮气含有的原子数目为 NA | |
| D. | 0.1 mol•L-1的Na2SO4溶液中含有Na+和SO42-的总物质的量为0.3 mol |
6.下列化合物的分子中,属于卤代烯烃的是( )
| A. | 乙烷 | B. | 甲苯 | C. | 乙 苯 | D. | 四氯乙烯 |
16.下列各溶液中,c(Na+)最大的是( )
| A. | 4 L 0.5mol/L的NaCl溶液 | B. | 2 L 0.8mol/L的NaOH溶液 | ||
| C. | 1 L 1mol/L的Na2CO3溶液 | D. | 0.5 L 1.2mol/L的Na2SO4溶液 |
3.设NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 2.4g镁的原子核外电子数为0.2NA | |
| B. | 2.3 g Na与氧气反应生成Na2O和Na2O2,转移电子数为0.1NA | |
| C. | 1mol丙烷分子中11 mol共价键 | |
| D. | 1.4 g C2H4和C3H6的混合气体中,含0.2NA的C原子 |
20.在不同条件或不同用量时,下列物质间发生化学反应产物不同的是( )
①AlCl3和NaOH溶液
②Na2CO3溶液和盐酸
③AgNO3溶液和氨水
④C和O2
⑤CO2 和NaOH溶液
⑥Fe和浓HNO3
⑦乙醇和O2.
①AlCl3和NaOH溶液
②Na2CO3溶液和盐酸
③AgNO3溶液和氨水
④C和O2
⑤CO2 和NaOH溶液
⑥Fe和浓HNO3
⑦乙醇和O2.
| A. | ①③⑤⑦ | B. | ②④⑥⑦ | C. | ③④⑤⑥⑦ | D. | 全部 |
1.有关有机物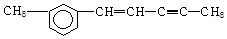 ,说法正确的是( )
,说法正确的是( )
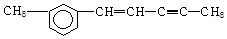 ,说法正确的是( )
,说法正确的是( )| A. | 该有机物属于脂肪烃 | |
| B. | 该有机物的分子式为:C12H14 | |
| C. | 该有机物可与5molH2发生加成反应 | |
| D. | 分子中,处于同一平面上的碳原子数最多可能有12个 |