题目内容
7.为了测定某有机物X的结构,做如下实验:①将该有机物完全燃烧,产物只有二氧化碳和水,元素组成分析发现,该物质中碳元素的质量分数为64.86%,氢元素的质量分数为13.51%;
②它的核磁共振氢谱有4组明显的吸收峰;
③它能与金属钠反应生成氢气.
试回答下列问题:
(1)有机物X的分子式为C3H8O;
(2)X的结构简式可能为CH3CH2CH2OH.
分析 由C与H的质量分数之和不是100%,燃烧产物只有二氧化碳和水,推断该有机物中含有O,且依据质量分数与相对原子质量之比求出各种元素的个数比,即可确定其分子组成,由含有4组吸收峰,说明含有四种不同环境的H,且含-OH,以此来解答.
解答 解:C与H的质量分数之和不是100%,燃烧产物只有二氧化碳和水,可知该有机物中含有O,
N(C):N(H):N(O)=$\frac{64.86%}{12}$:$\frac{13.51%}{1}$:$\frac{1-64.86%-13.51%}{16}$=3:8:1,
(1)由于H为8,C为3,满足3×2+2=8,故分子式为C3H8O,故答案为:C3H8O;
(2)它的核磁共振氢谱有4组明显的吸收峰,含4种H,能与金属钠反应生成氢气,可知含-OH,其结构简式可为CH3CH2CH2OH,故答案为:CH3CH2CH2OH.
点评 本题考查有机物的分子式计算的确定,为高频考点,把握元素质量分数确定原子个数比为解答的关键,侧重分析与应用能力的考查,注意饱和烃的结构特点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列说法正确的是( )
| A. | 碱金属元素随着核电荷数的增大,单质的溶沸点升高 | |
| B. | 卤族元素随着核电荷数的增大,单质的氧化性增强 | |
| C. | HF、HCl、HBr、HI的稳定性依次逐渐减弱 | |
| D. | LiOH、NaOH、KOH的碱性依次逐渐减弱 |
15.下列属于电解质的是( )
| A. | 铜 | B. | 生理盐水 | C. | 氢氧化钠 | D. | 乙醇 |
2.向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
| 操作 | 现象 | 结论 | |
| A | 滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+无K+ |
| C | 滴加氯水和CC14,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| D | 滴加几滴稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
12.下列叙述中正确的是( )
| A. | 氯化铝溶液中加入过量氨水反应的实质是Al3++3NH3•H2O═Al(OH)3↓+3NH4 | |
| B. | 存在于污水中的细菌,常用投加明矾等电解质的方法进行处理 | |
| C. | 镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液 | |
| D. | 依据铝热反应原理,能发生反应2Al+3MgO═3Mg+Al2O3 |
16.Al-H2O2电池可用于海上导航,该电池以碱性海水为电解质溶液,用铝和石墨做电极.下列说法正确的是( )
| A. | 负极反应Al-3e-=Al3+ | B. | H2O2在石墨电极上发生氧化反应 | ||
| C. | 石墨电极附近溶液的pH增大 | D. | 海水中的 OH ? 向正极移动 |
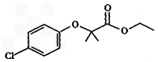


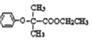 +Cl2$\stackrel{一定条件}{→}$
+Cl2$\stackrel{一定条件}{→}$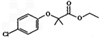 +HCl.
+HCl.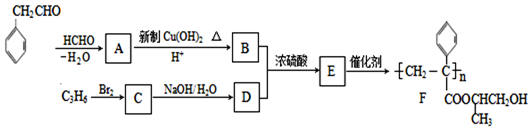
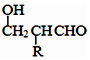 $\stackrel{-H_{2}O}{→}$
$\stackrel{-H_{2}O}{→}$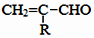
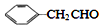 互为同系物,且G物质的相对分子质量比
互为同系物,且G物质的相对分子质量比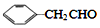 大14的,则符合下列条件的G的同分异构体有9种.
大14的,则符合下列条件的G的同分异构体有9种.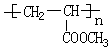 的合成路线
的合成路线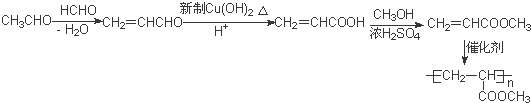 .
. A、B、C、D、E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示:
A、B、C、D、E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示: