题目内容
6.0.16g氢氧化钠恰好与20mL盐酸完全反应,则盐酸的物质的量浓度为( )| A. | 0.1mol•L-1 | B. | 0.2mol•L-1 | C. | 0.5mol•L-1 | D. | 1mol•L-1 |
分析 0.16g氢氧化钠物质的量n(NaOH)═$\frac{0.16g}{40g/mol}$=0.004mol,依据化学方程式定量关系计算得到HCl物质的量,溶液浓度c=$\frac{n}{V}$.
解答 解:16g氢氧化钠物质的量n(NaOH)=$\frac{0.16g}{40g/mol}$=0.004mol,HCl+NaOH=NaCl+H2O,得到n(HCl)=n(NaOH)=0.004mol,
20mL盐酸的物质的量浓度=$\frac{0.004mol}{0.020L}$=0.2mol/L,
故选B.
点评 本题考查了化学方程式、物质的量、物质的量浓度的计算分析,掌握基础是解题关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列物质中存在顺反异构体的是( )
| A. | CH3CH=CHCH3 | B. | CH2=CH2 | C. | 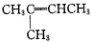 | D. | 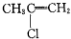 |
17.相同温度下,相同物质的量浓度的四种溶液:①CH3COONa,②NH4Cl,③NaHCO3,④Na2CO3.按pH值由大到小顺序排列正确的是( )
| A. | ④①③② | B. | ①④③② | C. | ①②③④ | D. | ④③①② |
14.X、Y为短周期元素,X位于IA族,X与Y可形成化合物X2Y,下列说法正确的是( )
| A. | X的原子半径一定大于Y的原子半径 | |
| B. | X与Y的简单离子不可能具有相同的电子层结构 | |
| C. | X2Y可能是离子化合物,也可能是共价化合物 | |
| D. | 两元素形成的化合物中,原子个数比不可能为1:1 |
1.下列说法正确的是( )
| A. | 增大反应物的量,化学反应速率一定加快 | |
| B. | 气体反应体系的压强增大,化学反应速率一定加快 | |
| C. | 与金属锌反应时,硫酸的浓度越大,产生H2速率越快 | |
| D. | 2molX气体在2L的容器中反应,4s后浓度变为0.5mol•L-1,则其反应速率为0.125mol•L-1•s-1 |
4.25℃时,已知Ksp(Ag2S04)=1.2×10-5,Ksp(AgCl)=1.8×10-10,Ksp(AgC2O4)=3.5×10-11,Ksp(AgI)=1.5×10-16,该温度下有关叙述正确的( )
| A. | AgCl、Ag2C2O4、AgI三者的饱和溶液中c(Ag+)大小顺序:Ag2C2O4>AgCl>AgI | |
| B. | 将0.02mol•L-1AgNO3溶液和0.02mol•L-1Na2SO4溶液等体积混合,有沉淀生成 | |
| C. | 向5mL饱和溶液AgCl溶液中滴加0.5mL0.1mol•L-1KI溶液,无沉淀生成 | |
| D. | 向浓度均为0.1mol•L-1的NaCl和KI混合溶液中滴加AgNO3溶液,先有白色沉淀生成 |
11.表中的数据表示破坏1mol化学键需要消耗的能量.计算1molH2(g)与O2(g)反应生成1molH2O(g)所释放的能量为245kJ.
| 化学键 | H-H | O-O | O═O | O-H |
| 能量(kJ) | 436 | 138 | 498 | 465 |
 已知X、Y、Z三元素的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.C、D是由X、Y、Z中两种元素组成的化合物,C通常状况下为无色液体,D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板.各物质之间的转换关系如图,部分生成物省略.
已知X、Y、Z三元素的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.C、D是由X、Y、Z中两种元素组成的化合物,C通常状况下为无色液体,D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板.各物质之间的转换关系如图,部分生成物省略.