题目内容
下列实验正确的是

A.配制一定浓度溶液 B.制取并收集Cl2 C.铁的析氢腐蚀 D.验证氨气易溶于水
【答案】
D
【解析】
试题分析:氢氧化钠固体不能直接倒入100mL容量瓶中溶解,应先在烧杯中溶解、冷却至25℃时,才能移入容量瓶中,且移液时一定要使用玻璃棒引流,故A错误;实验室常用二氧化锰和浓盐酸混合加热制取氯气,必须使用酒精灯加热,氯气的密度比空气大,必须用长进短出排气法收集,短进长出不能赶走集气瓶中的空气,故B错误;NaCl(食盐)是强酸强碱盐,食盐水呈中性,则铁、碳、中性电解质溶液形成原电池,发生吸氧腐蚀,在酸性环境中才可能发生析氢腐蚀,故C错误;氨气极易溶于水,瓶内气体压强迅速减小,瓶内外气体出现很大的压强差,若气球体积迅速增大,说明氨气易溶于水,故D正确。
考点:考查化学实验方案的设计与评价,涉及一定体积一定浓度溶液的配制、实验室制取并收集氯气、钢铁的吸氧腐蚀和析氢腐蚀、氨气的溶解性实验方案的设计与评价。

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
下列实验正确的是( )
| A、用湿润的pH试纸测定溶液的pH | B、用托盘天平称取11.7g NaCl晶体 | C、用碱式滴定管量取20.00mL的酸性KMnO4溶液 | D、用浓硫酸与NaOH溶液反应测定中和反应的反应热 |
下列实验正确的是( )
A、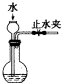 检查装置气密性 | B、 蒸发、浓缩、结晶 | C、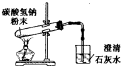 碳酸氢钠受热分解 | D、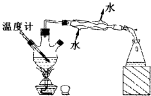 分离沸点不同且互溶的液体混合物 |