题目内容
下列化学用语正确的是( )
| A、乙炔的结构式是:C2H2 |
B、氟化氢的电子式: |
C、硫离子结构示意图: |
| D、氢氧化钡电离方程式:Ba(OH)2=Ba2++2OH- |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.乙炔分子中中含有1个碳碳三键、2个碳氢键,据此写出其结构式;
B.氟化氢为共价化合物,分子中不存在阴阳离子;
C.硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构;
D.氢氧化钡为强电解质,溶液中完全电离出钡离子和氢氧根离子.
B.氟化氢为共价化合物,分子中不存在阴阳离子;
C.硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构;
D.氢氧化钡为强电解质,溶液中完全电离出钡离子和氢氧根离子.
解答:
解:A.乙炔中碳原子最外层有4个电子,要达到稳定结构要形成四对共用电子对,而1个氢原子只能与1个碳原子形成形成1对公用电子对,所以碳原子和碳原子间只能形成3对公用电子对,所以乙炔的电子式为 ,将共用电子对换成短线即为结构式,乙炔的结构式为:H-C≡C-H,故A错误;
,将共用电子对换成短线即为结构式,乙炔的结构式为:H-C≡C-H,故A错误;
B.氟化氢分子中不存在阴阳离子,电子式中不能标出电荷,氟化氢正确的电子式为: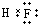 ,故B错误;
,故B错误;
C.硫离子的核外电子数为18,最外层为8个电子, 为硫原子结构示意图,硫离子结构示意图为:
为硫原子结构示意图,硫离子结构示意图为: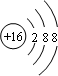 ,故C错误;
,故C错误;
D.氢氧化钡在溶液中完全电离出钡离子和氢氧根离子,其电离方程式为:Ba(OH)2=Ba2++2OH-,故D正确;
故选D.
 ,将共用电子对换成短线即为结构式,乙炔的结构式为:H-C≡C-H,故A错误;
,将共用电子对换成短线即为结构式,乙炔的结构式为:H-C≡C-H,故A错误;B.氟化氢分子中不存在阴阳离子,电子式中不能标出电荷,氟化氢正确的电子式为:
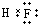 ,故B错误;
,故B错误;C.硫离子的核外电子数为18,最外层为8个电子,
 为硫原子结构示意图,硫离子结构示意图为:
为硫原子结构示意图,硫离子结构示意图为: ,故C错误;
,故C错误;D.氢氧化钡在溶液中完全电离出钡离子和氢氧根离子,其电离方程式为:Ba(OH)2=Ba2++2OH-,故D正确;
故选D.
点评:本题考查了电子式、电离方程式、离子结构示意图、结构式等化学用语的判断,题目难度中等,注意掌握常见化学用语的表示方法,明确离子结构示意图与原子结构示意图、结构式与结构简式的区别.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将氧化亚铁和硝酸铜的混合物9.08g全部溶解于含有0.3mol HCl的某浓度的盐酸中(此时有部分Fe2+被酸性条件下的NO3-氧化:3FeCl2+HNO3+3HCl═3FeCl3+NO↑+2H2O),放出标况下NO气体448mL.当向溶液中通入一定量的氯气时,溶液中的Fe2+刚好被完全氧化,再向溶液中加入10g过量的铁粉,充分反应后,有气体产生,过滤得不溶固体,下列叙述错误的是( )
| A、通入标准状况下Cl2的体积是448mL |
| B、放出标准状况下氢气的体积是224mL |
| C、FeO的质量是7.2g |
| D、得到不溶固体的质量是6.08g |
某校化学兴趣小组用如图所示过程除去AlCl3溶液中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失.

下列说法正确的是( )

下列说法正确的是( )
| A、NaOH溶液可以用氨水来代替 |
| B、溶液a中含有Al3+、K+、Cl-、Na+、OH- |
| C、溶液b中只含有NaCl |
| D、向溶液a中滴加盐酸需控制溶液的pH |
下列物质既能跟盐酸反应,又能跟NaOH溶液反应,还能跟H2O反应的是( )
| A、NH4Cl |
| B、NaAlO2 |
| C、NaHCO3 |
| D、Na2CO3 |
三种短周期元素在周期表中的位置关系如图所示,则关于A、B、C三种元素的叙述正确的是( )


| A、A的摩尔质量为8g/mol |
| B、B的最高价氧化物的化学式为HBO4 |
| C、C的一种氧化物为大气污染物 |
| D、三种元素中A的非金属性最强 |
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3
K2O+5Na2O+16N2↑,有关该反应说法正确的是( )
| ||
| A、属于复分解反应 |
| B、KNO3发生氧化反应 |
| C、NaN3是还原剂 |
| D、NaN3和KNO3中氮元素化合价均降低 |
下列各组有机物化合物中,肯定属于同系物的一组是( )
| A、C3H8与C5H12 |
| B、C4H6与C5H8 |
| C、C2H6O |
| D、C2H2与C6H6 |
下列实验能够成功的是( )
| A、只用溴水一种试剂可鉴别甲苯,乙烯,乙醇,四氯化碳四种液体 |
| B、淀粉用酸催化分解后的溶液中加入新制银氨溶液,水浴加热,可看到有银镜出现 |
| C、用乙醇,冰醋酸及1mol?L-1的H2SO4加热可制乙酸乙醇 |
| D、制取硝基苯时,向试管中加入试剂的顺序为:苯,浓硫酸,浓硝酸 |